*仅供医学专业人士阅读参考
最新研究进展速递~
2022年6月3-7日,一年一度的美国临床肿瘤学会(ASCO)年会召开,给全球癌症诊疗领域医生和从业者带来前沿、权威的学术盛宴。肺癌作为目前世界发病率和死亡率最高的恶性肿瘤之一,备受临床医生关注,在此次ASCO年会上亦有诸多研究进展公布。其中,在肺癌靶向治疗领域,除了大家比较熟悉的EGFR、ALK、NTRK、ROS1等驱动基因突变外,一些新兴的靶点也迎来了突破。让我们一起来了解下关于MET酪氨酸激酶结构域(MET TKD)突变的最新进展。
MET TKD突变:NSCLC靶向治疗的潜在新分子亚型
MET通路的异常激活可引起肿瘤的发生发展,MET通路异常的主要形式包括MET14号外显子跳跃突变、MET扩增、MET蛋白过表达和MET融合等。在2022年ASCO年会上公布的一项研究探索了一种罕见的分子亚型——MET TKD突变的发生情况、临床病理特征以及治疗方案(Abstract #9124)[1]。
该研究采用从一个多机构肿瘤队列的NSCLC病例中提取的临床病理学和基因组数据,这些肿瘤在GENIE v10、China Cancer和国际癌症基因组联盟/癌症基因组图谱(ICGC/TCGA)数据集中进行了基因组分析。同时,研究人员采用对来自Foundation Medicine基因组数据库的独立队列(包括NSCLC组织和液体样本),对MET-TKD突变率进行了外部验证。
研究结果显示,在整个队列(N=106,379)中,共662例样本(0.6%)检测出668个MET TKD突变(不伴MET14号外显子跳跃突变)(表1和图1)。
表1:整个队列中MET TKD突变和MET14号外显子跳跃突变的发生率
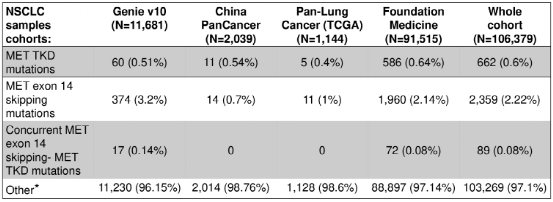
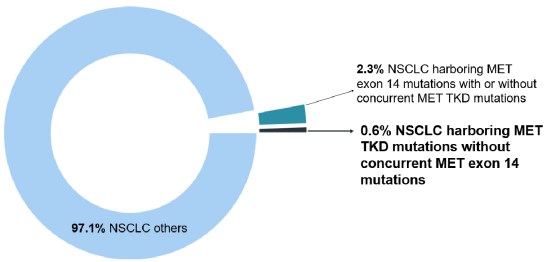
图1:整个队列中,与MET14号外显子跳跃突变相比,MET TKD突变(不伴MET14号外显子跳跃突变)的发生率
在这668个MET TKD突变中,525个突变的致病意义不明确,143个(21.4%)具有已知的致癌潜力,包括MET H1094Y/L/D/N/R、D1228N/H/V、L1995V/F、M1250T/I、Y1230H/C/G(图2A、B)。
在有完整基因组数据的携带MET TKD突变(不伴MET14号外显子跳跃突变)的662例NSCLC样本中,269例(41%)同时伴有KRAS、EGFR、ROS1、BRAF、ERBB2、ALK或RET驱动基因突变,393例(59%)无其他驱动基因共突变(图2 C),另外在28例(4.2%)样本中检测到MET扩增共同突变。
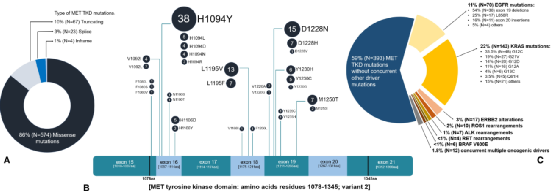
图2:NSCLC中MET TKD突变(不伴MET14号外显子跳跃突变)的特征
在人口统计学数据可用的患者中,与MET14号外显子跳跃突变NSCLC患者(N=390)相比,MET TKD突变NSCLC患者(N=75)明显更年轻(中位年龄63岁vs 73岁,p<0.0001),不过性别和自我报告的种族无显著差异。
专家简介
病例分享:研究人员还分享了2例MET TKD突变(未检测到其他驱动基因突变)NSCLC患者采用MET-TKI[Elzovantinib(TPX-0022)]治疗的疗效。其中1例为携带MET H1094Y突变的64岁男性肺腺癌患者,经Elzovantinib治疗后,肿瘤缩小-56.8%,达到部分缓解(图3A);另一例为携带MET F1200I突变的80岁男性NSCLC患者,治疗后肿瘤缩小-51.4%,亦达到部分缓解(图3B)。
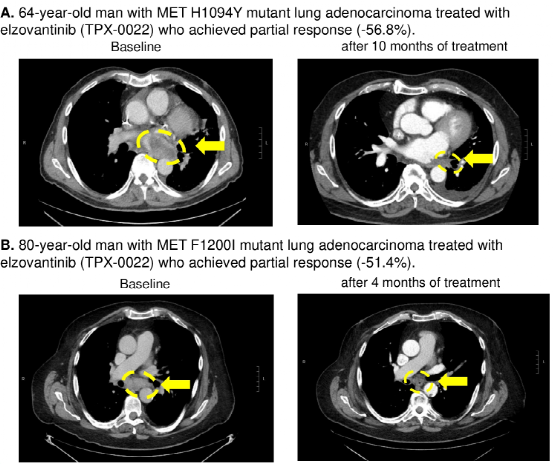
图3:MET TKD突变NSCLC患者采用Elzovantinib治疗的疗效
该研究结果表明,MET TKD突变(不伴MET14号外显子跳跃突变)在NSCLC中的检出率为0.6%,且通常不存在其他已知驱动基因突变共同突变。MET TKD突变可能是NSCLC中一种新的可靶向的分子亚型,而MET-TKI可能对此类患者有效。
MET通路异常,这些诊疗进展你要知道!
近年来,随着人们对MET通路异常认识的不断加深,MET靶向治疗得到了快速的发展。其中,MET14号外显子跳跃突变作为NSCLC的原发驱动基因,在总体患者中的发生率约为2%-3%[2],其中肺肉瘤样癌(PSC)中的发生率较高,为20%-31.8%[3,4]。目前,在国内外已有MET-TKI赛沃替尼、Capmatinib和Tepotinib获批该适应证,此外,谷美替尼等多种MET-TKI正在研发中。
研究数据[5,6]显示,赛沃替尼治疗MET14号外显子跳跃突变NSCLC患者的中位总生存期(OS)可达12.5个月,中位无进展生存期(PFS)为6.9个月,且客观缓解率(ORR,49.2%)和疾病控制率(DCR,93.4%)均较为优秀。另外,赛沃替尼起效迅速,中位起效时间为1.4个月。这些结果提示了赛沃替尼治疗的显著临床获益。
此外,在II期VISION研究[7]中,Tepotinib对MET14号外显子跳跃突变NSCLC患者具有持久的临床活性,总人群ORR为44.7%,安全性良好。GLORY研究[8]显示,谷美替尼的总人群的ORR为60.9%,初治患者的ORR略好于经治患者,分别为66.7%和51.9%,展现了较好的临床获益。而在2022年ASCO大会上公布的CHRYSALIS研究MET-2队列结果[9]显示,双特异性抗体类药物Amivantamab用于MET14号外显子跳跃突变NSCLC患者具有抗肿瘤活性,在既往未经治疗、既往未经MET抑制剂治疗和既往经MET抑制剂治疗患者中的ORR分别为57%、47%和17%。
在2022版《中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南》[10]中,在MET 14号外显子跳跃突变晚期NSCLC的用药推荐中,赛沃替尼获一线未用靶向治疗患者的治疗Ⅱ级推荐(3类证据),Capmatinib和Tepotinib获Ⅲ级推荐(3类证据)。同时,2022版CSCO指南的分子分型部分也将MET14号外显子跳跃突变检测由Ⅱ级推荐提升至Ⅰ级(3类证据),充分体现了MET14号外显子跳跃突变诊疗的重要性。
除了MET14号外显子跳跃突变外,MET扩增在NSCLC中亦备受关注。研究显示,MET扩增作为原发驱动基因,在初治患者中的发生率为1%-5%[2];作为继发驱动基因,在一/二代EGFR-TKI耐药后的发生率为5%-22%[11,12],在三代EGFR-TKI耐药后的发生率为15%-30%[13,14];作为共同驱动基因,在EGFR阳性初治患者中的发生率为2%-10%[15,16]。
目前,MET扩增NSCLC的治疗已经取得了诸多进展。比如,TATTON研究[17]已经初步证实了赛沃替尼联合奥希替尼双靶治疗MET扩增的EGFR-TKI耐药NSCLC患者的疗效和安全性;CHRYSALIS研究[18]中Amivantamab单药或联合Lazertinib治疗MET扩增的奥希替尼耐药NSCLC也显示出初步的疗效。
不过关于MET融合、MET过表达、MET TKD突变等MET通路异常,目前的循证医学证据仍然有限,未来希望随着更多研究的开展,为更多MET通路异常的患者带来有效的治疗方案。
参考文献:
[1]Activating MET kinase domain mutations define a novel molecular subtype of non–small cell lung cancer that is clinically targetable with the MET inhibitor elzovantinib (TPX-0022). 2022 ASCO, Abstract #9124.
[2]Guo R, et al. MET-dependent solid tumours - molecular diagnosis and targeted therapy.Nat Rev Clin Oncol. 2020;17(9):569-587.
[3]Tong JH, et al. MET Amplification and Exon 14 Splice Site Mutation Define Unique Molecular Subgroups of Non-Small Cell Lung Carcinoma with Poor Prognosis.Clin Cancer Res. 2016;22(12):3048-3056.
[4]Mo HN, et al. Targeting MET in cancer therapy.Chronic Dis Transl Med. 2017;3(3):148-153.
[5]Lu S, Fang J, Li X, et al. Once-daily savolitinib in Chinese patients with pulmonary sarcomatoid carcinomas and other non-small-cell lung cancers harbouring MET exon 14 skipping alterations: a multicentre, single-arm, open-label, phase 2 study[J]. Lancet Respir Med. 2021;9(10):1154-1164.
[6]S. Lu, J. Fang, X. Li, et al. Final OS results and subgroup analysis of savolitinib in patients with MET exon 14 skipping mutations (METex14+) NSCLC. 2022 ELCC. Abs 2MO.
[7]Xiuning Le, et al. Tepotinib Efficacy and Safety in Patients with MET Exon 14 Skipping NSCLC: Outcomes in Patient Subgroups from the VISION Study with Relevance for Clinical Practice[J]. Clin Cancer Res.2022;28 (6): 1117–1126.
[8]Shun Lu, Yongfeng Yu, Jianya Zhou, et al. Phase II study of SCC244 in NSCLC patients harboring MET exon 14 skipping (METex14) mutations (GLORY study). 2022 AACR. Abs CT034.
[9]Amivantamab in patients with NSCLC with MET exon 14 skipping mutation: Updated results from the CHRYSALIS study. ASCO 2022, Abs 9008.
[10]中国临床肿瘤学会指南工作委员会.中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南2021[M].北京:人民卫生出版社.
[11]Recondo G, et al. Targeting MET Dysregulation in Cancer. Cancer Discov. 2020;10(7):922-934.
[12]Bean J, et al. MET amplification occurs with or without T790M mutations in EGFR mutant lung tumors with acquired resistance to gefitinib or erlotinib. Proc Natl Acad Sci U S A. 2007;104(52):20932-20937.
[13]Ramalingam SS, et al. 2018 ESMO. Abstract LBA50.
[14]Wang Y, et al. Clinical analysis by next-generation sequencing for NSCLC patients with MET amplification resistant to osimertinib. Lung Cancer. Lung Cancer. 2018;118:105-110.
[15]Lai GGY, et al. Clonal MET Amplification as a Determinant of Tyrosine Kinase Inhibitor Resistance in Epidermal Growth Factor Receptor-Mutant Non-Small-Cell Lung Cancer. J Clin Oncol. 2019;37(11) 876-884.
[16]Li XM, et al. Clin Lung Cancer. 2020;S1525-7304(20)30334-X.
[17]Lecia V Sequist, Ji-Youn Han, et al. Osimertinib plus savolitinib in patients with EGFR mutation-positive, MET-amplified, non-small-cell lung cancer after progression on EGFR tyrosine kinase inhibitors: interim results from a multicentre, open-label, phase 1b study[J]. Lancet Oncol. 2020;21(3):373-386.
[18]Amivantamab monotherapy and in combination with lazertinib in post-osimertinib EGFR-mutant NSCLC: Analysis from the CHRYSALIS study. ESMO 2021, 1192MO.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |