*仅供医学专业人士阅读参考
刘洁琼教授带您详解艾立布林+阿帕替尼+卡瑞丽珠单抗三药联合研究价值!
三阴性乳腺癌(TNBC)作为预后最差的乳腺癌亚型,与其他亚型乳腺癌相比缺乏明确的治疗靶点,肿瘤侵袭性强,且常伴随内脏危象。患者一旦步入到晚期阶段后,有效治疗方案有限,总生存时间短,临床上亟待更多有效治疗方案。
2022年5月31日,国际顶级期刊Nature Communications在线发表了由中山大学孙逸仙纪念医院宋尔卫院士牵头、刘洁琼教授主导的一项探究艾立布林+卡瑞利珠单抗+阿帕替尼“艾立布林+靶免”组合三联治疗重度经治的晚期三阴性乳腺癌患者的多中心II期研究,为广大临床工作者带来了“E-base(以艾立布林为基础)”方案的最新数据。
医学界传媒就此特邀刘洁琼教授就该研究的重磅发现及临床意义进行分享,助力乳腺癌患者活得更好、活得更长。
选择高效低毒的联合化疗搭档,
亟待突破既往“靶免”不足
刘洁琼教授表示:“目前为止,免疫治疗仍无法完全满足TNBC的治疗需求。既往III期研究表明,免疫联合化疗一线治疗能够延长PD-L1阳性晚期TNBC患者的生存。然而对于PD-L1阴性患者,以免疫治疗为基础的后线治疗方案并未为患者带来生存获益。”
与此同时,既往研究显示,TNBC二线以及后线的选择和获益有限,单药及联合化疗的疗效并不理想。新型Trop-2 抗体偶联药物(ADC)为TNBC提供了新的治疗选择,但Trop-2 ADC的中位无进展生存期(PFS)仅为5.6个月。因此对于晚期TNBC的二线及后线治疗仍有着未被满足的治疗需求,临床工作者也开始了免疫相关探索[2-3]。
刘洁琼教授谈道:“遗憾的是,在晚期TNBC的二线及后线的治疗中,KEYNOTE-119等研究的相关探索均取得了阴性结果[4]。我们团队也就TNBC的免疫治疗进行了广泛研究,并于2022年在Clinical Cancer Research上发表了相关研究,结果显示,由于抗血管生成治疗能够改善免疫微环境,因此免疫联合抗血管生成治疗有着协同增效的作用,点燃了免疫治疗TNBC的新希望[5]。在此基础上,我们在II期研究中发现,PD-1单抗卡瑞利珠单抗联合抗血管生成药物阿帕替尼的‘去化疗’组合虽然在既往接受小于等于2线治疗的晚期TNBC患者中取得了43.3%的ORR,但患者的中位PFS仅为3.7个月,ORR获益并未能转化为患者的生存获益[6]。因此,我们认为有必要在免疫+抗血管生成方案的基础上进一步联合化疗。”
刘洁琼教授进一步谈道:“在化疗药物的选择方面,‘高效低毒’是联合治疗药物选择的标准。目前已有多项大型III期研究显示,艾立布林是晚期乳腺癌化疗的优选,在显著延长总人群 OS的同时对TNBC患者也有可观疗效。
艾立布林作为新一代微管抑制剂,具备独特的诱导肿瘤血管重塑的机制,能改善肿瘤血液灌注,提升抗肿瘤药物的组织渗透性,可达到改善免疫微环境和与其他药物协同增效的作用。同时,艾立布林的可感知不良反应发生率较低,对患者生活质量影响小,能够保障患者的用药耐受性。基于这两大特点,艾立布林更适用于联合治疗,并且基于既往艾立布林联合研究中所展现的疗效和安全性优势,我们认为艾立布林+阿帕替尼+卡瑞利珠单抗联合的“艾立布林+靶免”治疗模式能够让患者取得更多获益[7-11]。”
艾立布林加入“靶免”组合后疗效
实现突破,显著改善重度经治患者生存
就患者的基线特征,刘洁琼教授介绍道:“本研究入组的患者肿瘤负荷较大,普遍经历了多次治疗失败,患者的中位治疗线数为3线,最高者甚至达到10线,并且有17.4%的患者既往曾使用免疫联合化疗后疾病进展。此外,超过40%的患者存在肝转移。此外,本研究中很大一部分患者的无病间期(DFI)小于6个月,此前的IMpassion-130和KEYNOTE-355研究均未入组DFI小于6个月的患者。
而在这样基线状况较差的患者中,‘艾立布林+’方案仍取得了喜人的疗效。研究数据显示,在免疫+抗血管的“靶免”治疗基础上进一步引入艾立布林后,联合治疗的疗效得到了飞跃式提升。在意向治疗(ITT)人群中(46名),艾立布林+阿帕替尼+卡瑞利珠单抗“艾立布林+靶免”组合的ORR为37.0%,疾病控制率(DCR)高达87.0%。在生存数据方面,接受“艾立布林+靶免”组合治疗患者的中位PFS长达8.1个月,中位OS仍未达到。在安全性方面, 3/4级治疗相关不良反应(TRAE)的发生率仅为41.3%,主要为可防可控的中性粒细胞减少症、血小板减少症等,且三药之间没有交叉毒性的发生,耐受性较好[2]。”
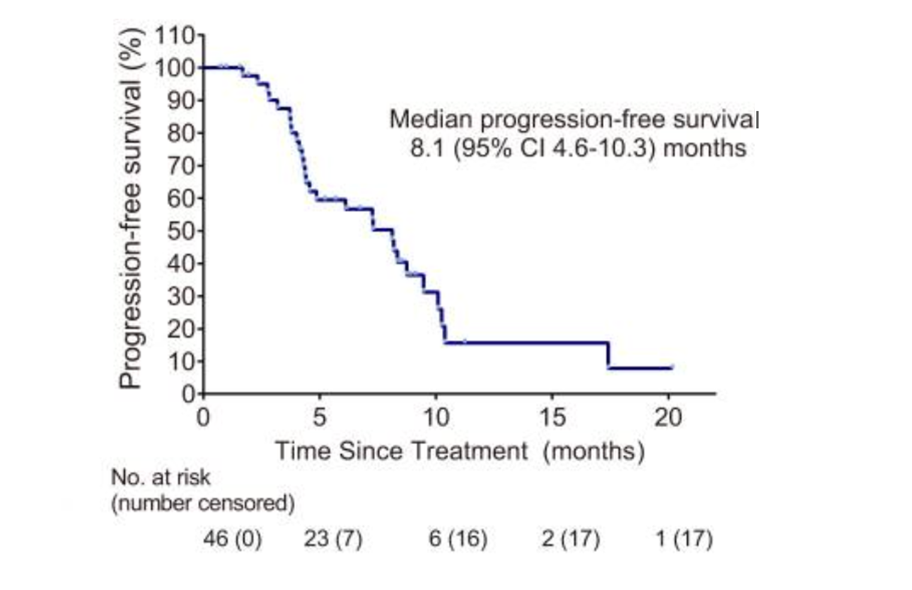
“艾立布林+靶免”方案PFS数据

“艾立布林+靶免”方案安全性数据
刘洁琼教授表示:“在‘靶免’组合的基础上加入艾立布林后,患者的生存得到了显著提升(中位PFS分别为8.1个月和3.7个月),艾立布林的加入使疾病缓解真正地转化为患者的切实生存获益。”
无论PD-L1表达,所有人群均可
在“艾立布林+靶免”方案下获益
刘洁琼教授谈道:“一项优秀的研究在疗效、安全性数据的基础上还需要完备的生物标志物分析。我们便基于艾立布林+阿帕替尼+卡瑞利珠单抗‘艾立布林+靶免’方案可观疗效的基础上进行了肿瘤标志物相关分析。其中针对PD-L1表达状态的分析显示,PD-L1 CPS评分与疗效之间不存在关联,无论患者PD-L1表达水平如何(阳性或阴性)均能从‘艾立布林+靶免’方案中获益。”
除此之外,此前多项发表于NATURE的研究均提示三级淋巴结构(TLS)与免疫治疗的疗效相关。本研究同样进行了TLS相关分析,结果显示,TLS更多(平均面积大≥30000μm²)患者的ORR显著高于TLS更少(平均面积<30000μm²)的患者(71.4% vs 25.0%)。虽然亚组分析同时发现患者的TLS与PFS没有显著关联,但TLS与ORR的关联仍提示TLS更多的患者可能更能从“艾立布林+靶免”方案中获益[2]。
刘洁琼教授谈道:“总的来说,本研究中进行了较为详细的生物标志物分析,进一步明确了‘艾立布林+靶免’治疗的获益人群,更加深入地贯彻了‘精准治疗’和‘个体化诊疗’的理念。”
医保助力,探索不止,
“艾立布林+靶免”方案望造福更多患者
刘洁琼教授总结道:“虽然本研究属于II期研究,但对于我国乃至全世界的晚期TNBC治疗领域均有重要的意义。首先,本研究中‘艾立布林+靶免’方案的疗效数据在数值上是所有相关前瞻性研究中最长的,其8.1个月的中位PFS数据远远大于既往研究中的相应数值。尽管不同研究中的数据无法直接进行对比,但本研究仍然证明了‘艾立布林+靶免’方案在晚期TNBC后线治疗中的疗效十分可观,并且‘艾立布林+靶免’方案的毒性相对较低。
目前艾立布林已被纳入医保,因此‘艾立布林+靶免’组合在经济条件有限的患者中仍有较高的可及性,进而能够惠及更多的患者。此外,本研究充分展现了E-base方案的潜力,希望未来有更多临床工作者能够探究艾立布林联合各类药物在各分子分型患者中的疗效和安全性,拓展艾立布林的应用场景,丰富艾立布林的应用依据,为乳腺癌患者带来切实的获益。”
刘洁琼教授表示:“这样一项极具意义研究的问世离不开多方的鼎力支持和通力协作,感谢宋尔卫院士的大力支持,也感谢本研究入组的所有患者及其家属。”
专家简介

宋尔卫 院士
中国科学院院士教授,主任医师,博士生导师,学科带头人
中山大学中山医学院院长.
中山大学孙逸仙纪念医院院长
逸仙乳腺肿瘤医院院长
中国抗癌协会乳腺癌专业委员会副主任委员
中国临床肿瘤学会(CSCO)乳腺癌专家委员会主任委员
中国医师协会外科医师分会乳腺外科医师委员会副主任委员
中国抗癌协会肿瘤转移专业委员会副主任委员
广东省医学会外科学分会副主任委员
何梁何利科学与技术创新奖,国家卫生计生突出贡献中青年专家,美国中华医学基金会(CMB)杰出教授,国家首批中青年科技创新领军人才,全国优秀科技工作者。
擅长乳腺癌根治手术,包括乳房切除术保乳的根治性手术;乳腺癌的辅助化学治疗、内分泌治疗以及晚期乳腺癌的综合治疗。主要从事乳腺癌早期诊断,包括BRCA1和BRCA2基因突变对家族性乳腺癌和血清蛋白指纹图对乳腺癌的早期诊断,以及乳腺癌的微创治疗和生物治疗,包括RNAF扰疗法等的研究。
专家简介

刘洁琼 教授
中山大学孙逸仙纪念医院乳腺外科副教授
中山大学孙逸仙纪念医院乳腺中心诊断科副主任
博士生导师(拟聘) 广东省杰出青年医学人才
2017年CSCO “35 under 35”最具潜力肿瘤医生
中华医学会肿瘤分会乳腺学组青年委员
CSCO转化医学专委员会委员
中国抗癌协会乳腺癌专业委员会青年学者
中国康复医学会修复重建外科专委会体表肿瘤学组委员
中国女医师协会肿瘤专委会委员
2008-2010哈佛大学麻省总医院联合培养博士
2014-2015年约翰霍普金斯医院乳腺中心博士后
以第一或通讯作者在PNAS、CCR 、JITC、NC等杂志发表SCI论文31篇,主持科研基金9项
参考文献:
[1]. National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology(Breast Cancer).Version 4.2022 — June 21, 2022.
[2]. Liu J, Wang Y, Tian Z, Lin Y, Li H, Zhu Z, Liu Q, Su S, Zeng Y, Jia W, Yang Y, Xu S, Yao H, Jiang W, Song E. Multicenter phase II trial of Camrelizumab combined with Apatinib and Eribulin in heavily pretreated patients with advanced triple-negative breast cancer. Nat Commun. 2022 May 31;13(1):3011.
[3]. Bardia A, Hurvitz SA, Tolaney SM, et al. Sacituzumab Govitecan in Metastatic Triple-Negative Breast Cancer. N Engl J Med. 2021 Apr 22;384(16):1529-1541.
[4]. Winer EP, Lipatov O, Im SA, et al. Pembrolizumab versus investigator-choice chemotherapy for metastatic triple-negative breast cancer (KEYNOTE-119): a randomised, open-label, phase 3 trial. Lancet Oncol. 2021 Mar 4.
[5]. Li Q, Wang Y, Jia W, et al. Low-Dose Anti-Angiogenic Therapy Sensitizes Breast Cancer to PD-1 Blockade. Clin Cancer Res. 2020 Apr 1;26(7):1712-1724. doi: 10.1158/1078-0432.CCR-19-2179.
[6]. Liu J, Liu Q, Li Y,et al. Efficacy and safety of camrelizumab combined with apatinib in advanced triple-negative breast cancer: an open-label phase II trial. J Immunother Cancer. 2020 May;8(1):e000696.
[7]. Kaufman PA, Awada A, Twelves C, et al. Phase III open-label randomized study of eribulin mesylate versus capecitabine in patients with locally advanced or metastatic breast cancer previously treated with an anthracycline and a taxane. J Clin Oncol. 2015 Feb 20;33(6):594-601.
[8]. Wu Y, Wang Q, Zhang J, et al. Incidence of peripheral neuropathy associated with eribulin mesylate versus vinorelbine in patients with metastatic breast cancer: sub-group analysis of a randomized phase III study. Support Care Cancer. 2020 Aug;28(8):3819-3829.
[9]. Cortes J,O'Shaughnessy J,Loesch D,et al.Eribulin monotherapy versus treatment of physician's choice in patients with metastatic breast cancer(EMBRACE):a phase 3 open-label randomised study[J].Lancet.2011;377(9769):914-23.
[10]. Kaufman, P. A. et al. Phase III open-label randomized study of eribulin mesylate versus capecitabine in patients with locally advanced or metastatic breast cancer previously treated with an anthracycline and a taxane. J Clin Oncol (33): 594-601.
[11]. Yuan P, et al. Eribulin mesilate versus vinorelbine in women with locally recurrent or metastatic breast cancer: A randomised clinical trial. Eur J Cancer. 2019 May(112):57-65.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |