*仅供医学专业人士阅读参考
肺癌精彩病例分享,一键查收!
患者初诊为驱动基因阴性的右肺腺癌伴右侧支气管旁淋巴结转移、右肺内转移、胸膜转移、左肺磨玻璃灶(恶性可能)(cT4N1M1b,IV期)。患者接受培美曲塞+卡铂+贝伐珠单抗4个周期,疗效评估疾病稳定(SD)。治疗期间组织基因检测结果显示该患者为EGFR 21号外显子L858R突变、EGFR扩增。一线治疗4周期后换用吉非替尼+贝伐珠单抗维持治疗,疗效评估为部分缓解(PR),无进展生存期(PFS)为3年10个月。患者右肺结节较前缓慢增大,为患者加大吉非替尼剂量,但疗效不佳,治疗9个月后患者进行血液二代测序(NGS)检测未见T790M突变,之后更换为奥希替尼+贝伐珠单抗,疗效评价为SD。
治疗4个月后肺部残留病灶行射频消融,术前行肺穿刺活检证实腺癌,组织基因检测提示患者为EGFR 21号外显子 L858R突变、MET 14号外显子跳跃突变。患者接受赛沃替尼+奥希替尼双靶治疗,PFS大于9个月。截至目前,患者总生存期(OS)接近6年。该病例由大连医科大学附属第一医院王阿曼教授提供,并邀请大连医科大学附属第一医院刘基巍教授点评。
病例简历
基本情况:
患者男,63岁,2016年4月因“干咳伴右侧胸痛3月,发热10天”就诊于我院呼吸科。
既往史:2015年诊断房颤行射频消融术,2000年因阑尾炎行阑尾切除术。
个人史:吸烟10年,10支/日,2015年戒烟。
2014年3月27日体检胸部CT:左肺尖磨玻璃影(8.9mm),右肺斑片影(3cm)。
2015年5月6日胸部HRCT:右肺上叶水平裂旁斑片影,恶性不除外,水平裂旁结节较前增多、增大,左肺尖磨玻璃影较前相仿,恶性不除外。
2016年4月8日胸部CT:右肺上中叶水平裂区可见一团片状高密度影,3.3cm*2.4cm,形态不规则,部分与胸膜联系紧密,考虑炎症病变可能性大;左肺上叶尖后段见斑片状混杂密度磨玻璃影,边界不清,可见浅分叶,临近胸膜受牵拉,考虑微浸润性腺癌。
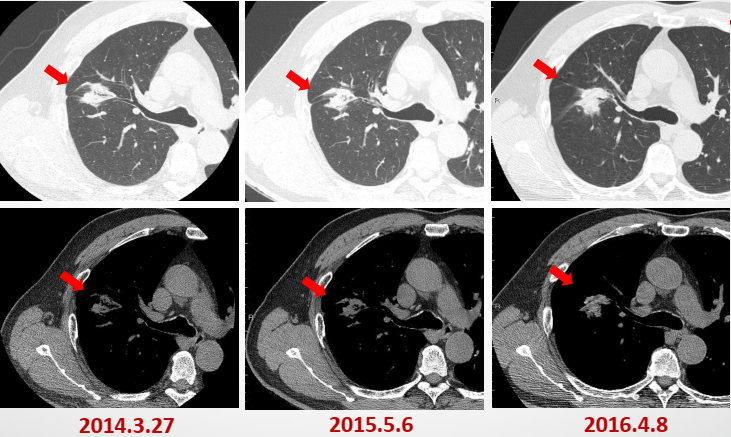
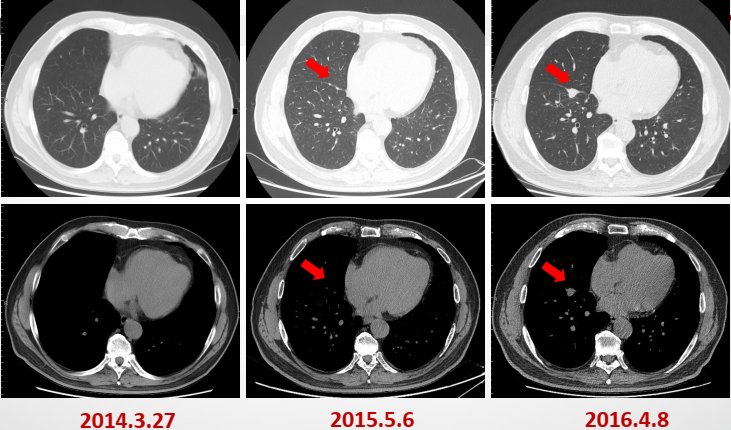
图1. 2014年3月27日(左)、2015年5月6日(中)、2016年4月8日(右)胸部CT检查结果
2016年5月4日PET/CT:右肺上叶团片灶,FDG代谢明显增高,首先考虑肺癌;右中间段支气管旁FDG代谢增高淋巴结;右侧7、8肋软骨周围、右侧第9、11后肋FDG代谢增高灶;右肺叶间裂旁多发结节,部分FDG代谢增高,均首先考虑转移瘤;左肺尖磨玻璃灶,未见FDG代谢增高。
2016年5月6日超声气管镜(EBUS):未探及右肺上叶病灶。
灌洗液涂片细胞学病理示:见腺癌细胞。
血液NGS检测:未见明确驱动基因突变。
诊断结果:右肺腺癌(cT4N1M1b,IV期),驱动基因阴性,右侧支气管旁淋巴结转移、右肺内转移、胸膜转移,左肺磨玻璃灶(恶性可能)。

患者初诊为驱动基因阴性的右肺腺癌伴右侧支气管旁淋巴结转移、右肺内转移、胸膜转移、左肺磨玻璃灶(恶性可能)(cT4N1M1b,IV期)。2016年8月,患者接受培美曲塞+卡铂+贝伐珠单抗一线治疗4个周期,疗效评估为缩小的SD。治疗期间进行组织基因检测,结果显示患者为EGFR 21号外显子L858R突变、EGFR扩增。因此,患者从2016年9月4日开始改为EGFR抑制剂吉非替尼联合贝伐珠单抗维持治疗,期间不良反应可控,疗效评估为PR,PFS为3年10个月。
2020年7月复查显示患者右肺结节较前缓慢增大,为患者加大吉非替尼剂量为500mg Qd po,但疗效不佳,2020年10月20日、2021年4月16日复查结果显示患者右肺结节缓慢增大。2021年4月26日患者进行血液NGS检测未见T790M突变,之后更换为奥希替尼+贝伐珠单抗治疗,疗效评价为SD。
2021年8月25日患者治疗4个月后肺部残留病灶行射频消融,术前行肺穿刺活检证实腺癌,组织基因检测提示EGFR 21号外显子L858R突变、MET 14号外显子跳跃突变。2021年9月26日患者开始接受奥希替尼联合赛沃替尼双靶治疗治疗,不良反应可控,PFS大于9个月。2022年2月15日、2022年5月12日复查显示患者右侧胸腔积液较前增多,余病灶稳定。近两月患者行2次胸腔穿刺术,见淡血性胸腔积液,胸水细胞学病理示恶性积液,胸腔注射贝伐珠单抗联合卡铂治疗,但胸水控制可,目前继续双靶治疗。
病例提供专家
王阿曼教授:动态基因检测实现精准治疗,助力患者实现长生存
在我国非小细胞肺癌(NSCLC)患者中,约一半存在EGFR突变。近年来,随着EGFR-TKI不断迭代,EGFR突变NSCLC患者的生存时间也逐渐延长。本例患者初诊时采用血液 NGS检测,结果为驱动基因阴性,一线治疗选择了化疗联合抗血管生成治疗,疗效评估为SD。在一线治疗期间,患者进行了组织NGS检测,结果显示患者为EGFR 21号外显子L858R突变、EGFR扩增。在接受四个周期一线治疗以后,患者改为吉非替尼联合贝伐珠单抗维持治疗,使患者不错过靶向治疗机会,PFS达到了3年10个月。
除了常规的EGFR、ALK基因的检测之外,MET14号外显子跳跃突变也是重要的原发致癌驱动基因变异,在肺癌中的发生率约为3%-4%[1]。美国国家综合癌症网络(NCCN)[2]、中国临床肿瘤学会(CSCO)[3]等国内外多个指南均推荐NSCLC患者常规检测MET14号外显子跳跃突变。本例患者第二次进行组织NGS检测时,结果显示患者出现EGFR-TKI继发性耐药,存在EGFR 21号外显子L858R突变以及MET14号外显子跳跃突变。采取奥希替尼以及赛沃替尼双靶治疗后,患者的PFS超过9个月,且安全性可控。
在精准治疗时代,精准检测是前提,精准检测能够为后续治疗方案选择提供准确的指导,本例患者在治疗的过程中通过动态基因检测,针对驱动基因采取精准治疗措施,使患者获益最大化,并且获得长生存的可能,这也提示我们临床中动态基因检测的重要性。
专家点评
刘基巍教授:赛沃替尼改写中国MET靶点治疗格局,双靶治疗前景可期
本例患者为存在EGFR第21外显子L858R突变以及MET14号外显子跳跃突变的共突变IV期肺癌患者,在既往的治疗中比较少见。存在MET基因突变的NSCLC患者,化疗效果远低于驱动基因阴性的患者,OS较短。即使合并PD-L1有高表达,对免疫治疗反应不佳。在EGFR-TKI继发性耐药后,该患者需要精准且高效的药物治疗策略。
2021年6月22日,赛沃替尼在中国获批上市,用于治疗存在MET14号外显子跳跃突变的局部晚期或转移性NSCLC患者。赛沃替尼打破了以往MET位点无药可用的困境,为中国MET突变患者提供了全新的治疗选择。在2021版的《CSCO非小细胞肺癌诊疗指南》上,赛沃替尼也被列为治疗MET14号外显子跳跃突变的II级推荐用药。
赛沃替尼治疗MET14号外显子跳跃突变肺肉瘤样癌或其他NSCLC亚型的Ⅱ期临床研究结果显示,在肿瘤疗效可评估集(TRES)中,赛沃替尼治疗的ORR为49.29%,疾病控制率(DCR)为93.4%,中位PFS为6.9个月,中位OS为12.5个月[4,5]。该研究提示,赛沃替尼对于MET14号外显子跳跃突变NSCLC患者具有确切的疗效。同时,在该研究中赛沃替尼展现了良好的安全性和耐受性,治疗相关不良反应多为1-2级。赛沃替尼的安全性在本例患者的治疗过程也得到了印证,患者后线采用奥希替尼联合赛沃替尼双靶治疗,不良反应可控。
目前也有许多研究正在探索奥希替尼联合赛沃替尼用于奥希替尼治疗进展的EGFR与MET共突变的患者的疗效和安全性,未来随着研究结果的陆续公布,将进一步积累双靶治疗的证据,更有助于指导临床实践。
目前患者新发胸腔积液,细胞学病理证实为恶性积液,胸水细胞蜡块未见MET14号外显子跳跃突变,后续仍需进一步调整治疗方案,为患者谋求长期生存的可能性。希望未来越来越多像赛沃替尼这类高效、低毒的药物能够投入临床实践中,为更多的肺癌患者治疗改善生存现状。
病例点评专家简介

刘基巍 教授
大连医科大学附属第一医院
肿瘤学教研室主任,肿瘤一科主任
中国临床肿瘤学会(CSCO)常务理事
CSCO-肿瘤心脏病学专业委员会主任委员
CSCO-小细胞肺癌专业委员会副主任委员
CSCO-黑色素瘤专业委员会副主任委员
国家卫计委肿瘤合理用药专家委员会专家
中华医学会肿瘤分会肿瘤内科专委会委员
中国抗癌协会抗肿瘤药物研究专委会委员
从事肿瘤临床医疗、教学和科研近三十年,曾于日本国 北九州国立癌症中心、美国西北大学Rorbert H.Lurrie肿瘤中心学习深造。
病例提供专家简介

王阿曼 教授
副主任医师,肿瘤学博士
就职于大连医科大学附属第一医院肿瘤科
中国临床肿瘤学会(CSCO)胆道肿瘤专委会委员
CSCO肿瘤心脏病学专委会委员
中国抗癌协会中西医整合肿瘤专业委员会青年委员
辽宁省细胞生物学会精准医学和大数据专业委员会委员
辽宁省营养学会肿瘤营养专委会委员
大连肿瘤学会委员
首届CSCO 35 under 35最具潜力青年肿瘤医生全国百强
主持国家自然基金青年基金1项、辽宁省博士启动基金1项
以第一作者发表论文14篇,其中SCI论文7篇,参编著作1部
参考文献:
[1]非小细胞肺癌分子病理检测临床实践指南(2021版)[J].中华病理学杂志,2021, 50(4):323-332.
[2]NCCN Clinical Practice Guidelines in Oncology:Non-Small Cell Lung Cancer. Version 1. 2022.
[3]中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南2021版.
[4]Lu S, Fang J, Li X, et al. Once-daily savolitinib in Chinese patients with pulmonary sarcomatoid carcinomas and other non-small-cell lung cancers harbouring MET exon 14 skipping alterations: a multicentre, single-arm, open-label, phase 2 study[J]. The Lancet Respiratory Medicine, 2021, 9(10): 1154-1164.
[5]Lu S, Fang J, Li X, et al. 2MO Final OS results and subgroup analysis of savolitinib in patients with MET exon 14 skipping mutations (METex14+) NSCLC[J]. Annals of Oncology, 2022, 33(S2): S27.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |