*仅供医学专业人士阅读参考
结果令人惊喜!
作为血液和肿瘤学领域最为顶级的学术会议,每年6月的美国肿瘤学会(ASCO)年会和欧洲血液学会(EHA)都会传递全球最新最重磅的研究进展。每年这两大会议都会接受全世界优秀的原创研究投稿,因此入选口头报告的竞争异常激烈,其结果也备受关注。
以今年为例,ASCO年会共有5198篇摘要投稿,而EHA年会共有2239篇,其中与多发性骨髓瘤相关的摘要分别有168篇和332篇。最终,选入ASCO口头发言的多发性骨髓瘤摘要仅13篇,选入EHA的也仅25篇,其入选难度可想而知。
而在今年的ASCO年会和EHA年会上,我国有一项基于FasT CAR-T平台治疗多发性骨髓瘤的原创研究同时入选2个大会的口头报告环节,它就是海军军医大学第二附属医院(上海长征医院)血液科杜鹃教授代表团队汇报的BCMA/CD19双靶点快速CAR-T疗法GC012F治疗复发/难治性多发性骨髓瘤(R/R MM)多中心首次人体研究的最新结果。
这项研究为何会同时受到ASCO和EHA这两个国际顶尖大会的青睐?这项研究对疾病治疗领域有哪些深远的影响和意义?带着这些问题,医学界血液频道对话杜鹃教授,试图为大家讲解这项口头报告背后的“故事”。
数据“惊艳”:疗效和安全性“双优”
这个研究的“主角”——GC012F是一种B细胞成熟抗原(BCMA)和CD19双靶向自体CAR-T产品,基于FasTCAR平台技术进行研发,具备“次日完成生产”的优势,仅需22-36小时即可制备完成。在临床前和首次人体试验的前期结果中,GC012F已持续展示出卓越的安全性与有效性,目前在研的适应证包括多发性骨髓瘤及B细胞非霍奇金淋巴瘤。2021年11月,GC012F被美国食品药品监督管理局(FDA)授予孤儿药资格认定,用于治疗多发性骨髓瘤。
此次在6月份的ASCO和EHA年会上,杜鹃教授研究团队提供了在较长随访时间下GC012F的最新安全性和初步疗效数据。
这项单臂、开放标签、多中心的研究者发起试验(IIT)共纳入29名年龄27-76岁的R/R MM患者,给予单次输注GC012F治疗。
这些患者中,平均既往治疗线数为5线(范围2-9),89.3%为高危组(HR-mSMART),8例伴随EM疾病,3例从未(包括移植后)达到完全缓解(CR),24例对最后治疗难治,3例原发难治,9例既往接受过抗CD38治疗,27例接受过免疫调节药物(IMiDs)治疗,26例PI难治,26例IMiDs难治。“从临床特点可以看得出来,纳入研究的都是既往治疗相对比较棘手的一些多发性骨髓瘤患者。”杜鹃教授说。
经过2-3天的清淋化疗(30mg/m2/d,300mg/m2/d Flu/Cy)后,GC012F按3个剂量水平单次输注:1x105/kg(2例),2x105/kg(10例)和3x105/kg(16例)。
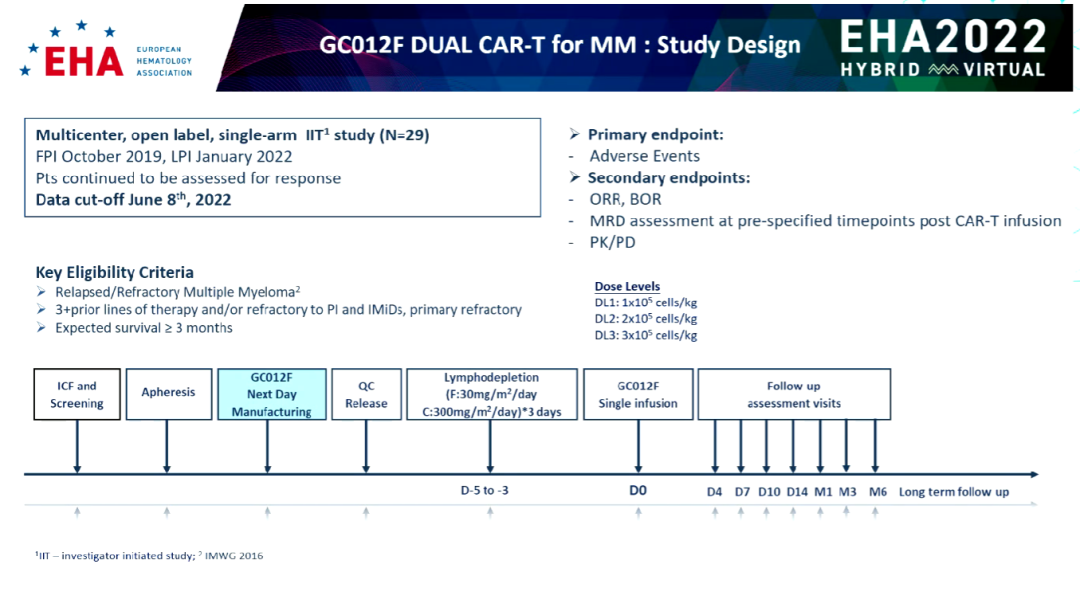
图1:研究设计(来源:EHA大会报告)
截止2022年6月,中位随访时间为11个月(范围4.9-34.5),研究发现:
①总缓解率(ORR)达到93%,疾病缓解深度良好:3个剂量组的ORR分别为100%(2/2)、80%(8/10)和93.8%(15/16),总体为93%(图2)。29例患者中,27例可评估患者微小残留病灶MRD(经流式细胞术灵敏度104-106)均达到了阴性(100%)(图3)。第28天评估时,81.5%的可评估患者MRD阴性。75%的患者(21/28例)达到了MRD-sCR(MRD阴性-严格意义上的完全缓解)。数据截止时,中位疾病缓解时间(mDoR)为15.7个月。
杜鹃教授补充道:“如果我们以欧洲EuroFLOW的106为MRD阴性界值,有87.5%的患者在治疗1年后仍在MRD阴性(图4),说明缓解的持续时间也非常理想。此外,由于最后1个入组的患者只有5个月的随访时间,随着随访时间的延长,我们相信疾病缓解时间肯定还会更好,结果更让人期待。”
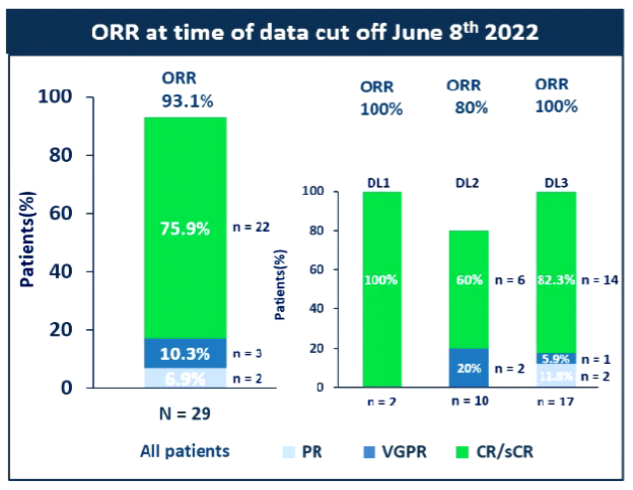
图2:截止2022年6月8日,疾病总缓解率为93.1%(来源:EHA大会报告)
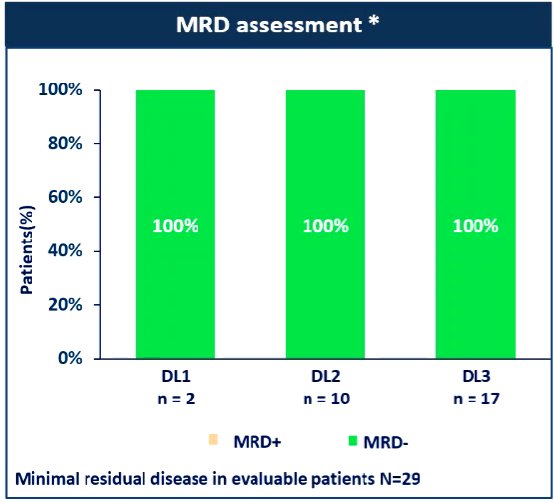
图3:3个剂量组的MRD阴性率均达到100%(来源:EHA大会报告)
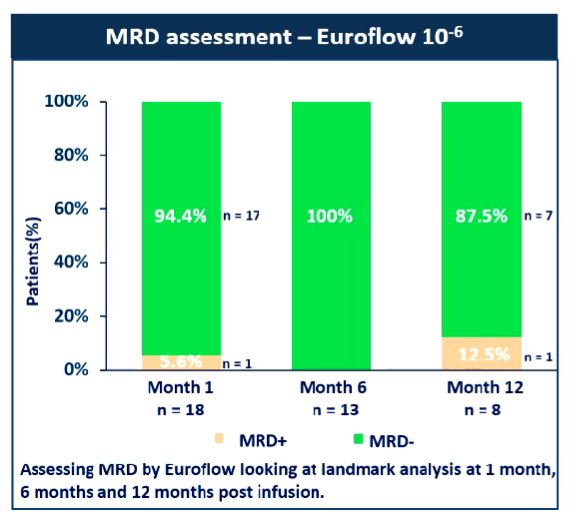
图4:以Euroflow10-6为MRD评估界值,治疗后1年MRD阴性率为87.5%(来源:EHA大会报告)
②治疗安全性良好:全部29名患者中,3名未出现细胞因子释放综合征(CRS),23例的CRS反应为1-2级,2例患者达到3级,未观察到4/5级的CRS。CRS的中位持续时间为3天(范围1-8)。同时,未观察到神经系统毒性ICANs。
③CAR-T细胞体内扩增状态和持续时间良好:药代动力学(PK)结果显示,剂量水平之间无差异。总的来说,CAR-T的中位达峰时间(Tmax)为10天(范围8-14),中位峰值拷贝数(Cmax)为97009(16011-374346)拷贝/ug DNA,最长持续时间达到793天(数据截止)。3个剂量组CAR-T几何平均AUC0-28分别为468863,631540和581620拷贝day/μg genomic DNA。
“总体来说,GC012F在所有的患者的体内扩增状态非常好,持续时间比较长。”杜鹃教授评价道。
因此,研究结果表明:基于新FasT CAR平台下的双靶点CAR-T,不仅制备快速,而且治疗复发难治多发性骨髓瘤患者其缓解深度和持续时间表现优异,安全性良好。“应该说这项研究对将来这种CAR-T在临床上的应用,特别是在双靶CAR-T的领域,有了一个初步的探索,给大家提供了确凿的临床数据支持。”杜鹃教授说。
源头创新:从基础到临床
这项研究为何能受到国际学者的关注?除了其优异的临床疗效外,值得一提的是疗法的创新:双靶及快速生产。
杜鹃教授如此解释:“BCMA在整个浆细胞都有广泛的表达,而CD19可以在更早的祖细胞阶段表达。以往多发性骨髓瘤的CAR-T多基于BCMA单靶点,治疗后仍然会有患者复发或进展,这是一个无法克服的难题。这次我们在CAR-T制备过程中将两个靶点联合在一起,同时靶向不同的抗原,那么就可能能够克服CAR-T的耐药问题,减少脱靶效应,从而达到加深的疾病缓解,更持久的治疗疗效。
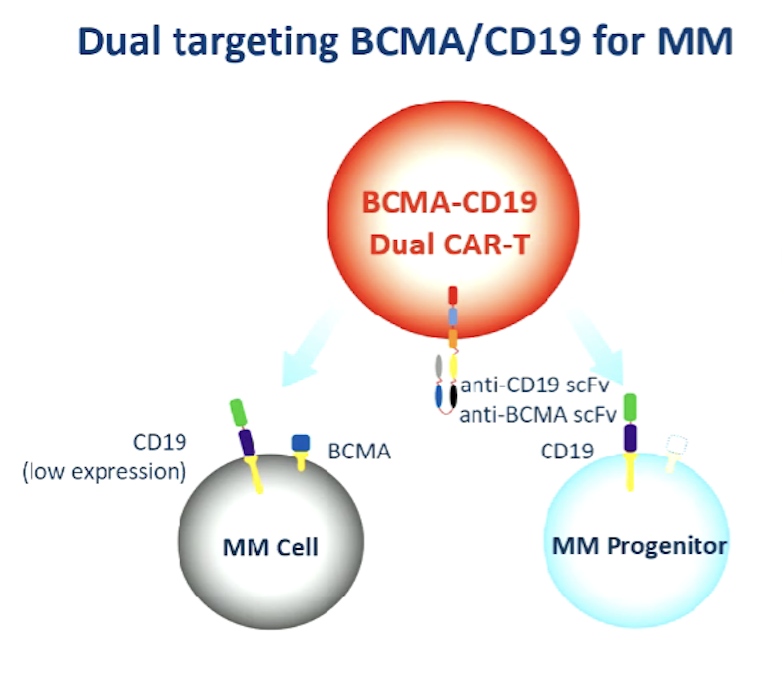
图5:BCMA/CD19双靶点CAR-T治疗多发性骨髓瘤的原理图(来源:EHA大会报告)
同时,基于FasT CAR的平台CAR-T疗法,它的制备速度非常快,而这种检测的流程比传统CAR-T也能节省近50%-70%的时间。
目前,CAR-T治疗的骨髓瘤患者的临床研究均为复发或难治阶段患者,传统CAR-T往往耗时较长,在等待过程中大多患者还要接受桥接治疗,并且回输之前对于接受桥接治疗患者还需要洗脱期。而使用快速的制备方法,一方面可以节省治疗的等待间歇期,同时它是体内扩增的双靶点CAR-T,临床疗效似乎比传统CAR-T更加理想,安全性高,是一种非常具有前景的CAR-T疗法。”
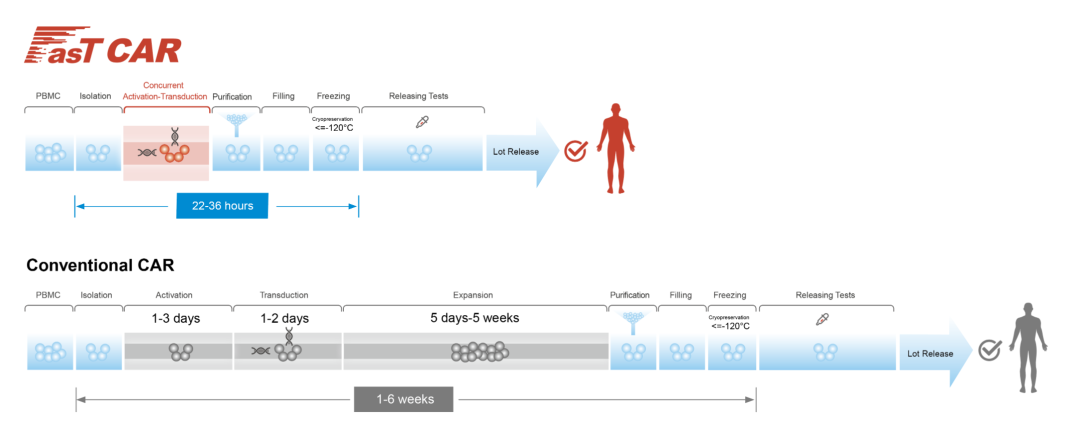
图6:FasTCAR平台基本原理及与传统CAR平台的对比(来源:亘喜生物官网)
目前,复发/难治的多发性骨髓瘤一直是血液肿瘤临床上的重点和焦点领域。近年来,随着多种新药和新疗法的应用和上市,这类患者的治疗选择越来越多。同时,不少血液肿瘤临床机构都在开展相应的临床试验。
作为在血液肿瘤领域内有丰富治疗经验的专家,杜鹃教授也谈到:“这几年来,多发性骨髓瘤的治疗理念更新发展迅速。新药层出,也有多种不同机制的药物,如达雷妥尤单抗、泊马度胺、卡非佐米,XPO-1、BCL-2抑制剂、BCMA双抗,ADC药物等,但是这些药物如何配比和治疗方案选择的先后顺序是很重要的科学问题。对于复发难治患者,应当首先考虑纳入临床试验中,既能让患者有机会接受最新的药物治疗,也能节省经济的压力。因此,以CAR-T为代表的临床试验的确给复发难治骨髓瘤患者带来新的契机,帮助很多患者解决难题。我们也非常期待,这样的临床疗法能够早一点在国内获批上市,同时希望它的价格能更加亲民,让更多的患者能够从CAR-T疗法中获益。”
精彩纷呈:多发性骨髓瘤新进展
除了这项研究之外,在今年的ASCO和EHA年会上,多发性骨髓瘤领域内的其他不少口头报告也同样值得关注。
杜鹃教授总结:“在骨髓瘤治疗方面,研究者主要聚焦初诊和复发难治这两个群体的患者。在治疗方法上,一方面骨髓瘤治疗的主流药物或者基石方案研究更新,例如药物不同组合策略,更长时间随访,以及造血干细胞移植的地位;另一方面就是治疗新药,包括双靶点抗体、ADC、CAR-T等新型疗法大放异彩。”
针对新诊断多发性骨髓瘤(NDMM)患者,被纳入EHA年会LBA(Late-Breaking Abstract)DETERMINATION研究(LB2366)报告了NDMM患者接受RVd(来那度胺、硼替佐米、地塞米松三联疗法)后序贯自体造血干细胞移植(ASCT)的安全性和有效性。研究显示,与未接受ASCT的患者相比,接受ASCT的患者,虽然OS未见明显差异,但无进展生存期(PFS)显著改善。
而在复发难治性多发性骨髓瘤(R/R MM)的双特异性抗体治疗领域,MajesTEC-1研究结果显示,无论R/R MM患者既往是否接受过抗BCMA治疗,都能够从BCMA/CD3双特异性抗体Teclistamab的治疗中获得深度和持久的缓解,而且CRS不良反应都相对可控,大多数都在1-2级。此外另一个BCMA/CD3双抗Elranatamab的相关研究MagnetisMM-3也显示出不错的总体有效率和安全性。
另一种靶向GPRC5D/CD3的新型双特异性抗体药物Talquetamab相关的MonumenTal-1研究最新结果提示,对既往经多线治疗的RRMM也可能有非常良好的治疗前景。
此外在CAR-T治疗方面,除美国已上市CAR-T产品公布相关真实世界研究数据外,我国学者也都有重磅研究公布,包括人源性CAR-T及靶向GPRC5D的CAR-T等等。
另外,由于新型抗体偶联物(ADC)Belantamab Mafodotin在美国已经获批上市,此次EHA会议也展示了其联合RD治疗NDMM患者的安全性和有效性。
“从国际会议的口头报告可以看出,多发性骨髓瘤治疗进展的确是让人非常惊喜,也体会到了新药物和新疗法所带来的魅力。并且,在这样一个全球顶级的盛会看到我们中国学者的多项研究的展示,体现了我国骨髓瘤事业的发展和进步,也期待未来我们有更多原创的研究成果在国际舞台展示,给世界带来惊喜,为骨髓瘤治愈的目标添砖加瓦。”杜鹃教授最后说道。
专家简介

杜鹃 教授
海军军医大学第二附属医院(上海长征医院)血液病科主任、全军骨髓瘤和淋巴瘤疾病中心主任。主任医师、教授、博士研究生导师。先后获得德国乌尔姆大学医学和东南大学理学双博士学位。先后入选上海浦江人才计划,上海市第八届青年科技英才,深蓝人才工程“领航”人才,2021年获得“全国人民好医生(血液肿瘤)青年典范”。担任国际骨髓瘤工作组专家委员会委员,亚洲骨髓瘤工作网委员(AMN),中华医学会血液学分会全国青年委员,中国医师协会血液学分会多发性骨髓瘤专业委员会委员等任职。同时还担任国内外多部血液病期刊审稿专家、执笔或参加撰写多部国内、外骨髓瘤疾病相关指南。
长期致力于血液肿瘤的临床和科研一线工作,深耕细作、突破创新。围绕复发难治多发性骨髓瘤的靶向治疗、CAR-T细胞免疫治疗、罕见浆细胞疾病等领域深入探索,注重临床和基础研究的相互转化。先后承担近20余项科研项目,包括国家自然科学基金5项,国际骨髓瘤基金会(IMF)项目2项。以第一作者或通讯(共同)作者先后发表SCI论文20余篇,包括Blood、Leukemia、Haematologica等血液领军杂志(单篇最高影响因子22.113分)。
本文首发:医学界血液频道
本文作者:渝小苏
本文审核:上海长征医院 杜鹃
责任编辑:Sweet
| 留言与评论(共有 0 条评论) “” |