仅供医学专业人士阅读参考
心肾相交?复杂而又重要的病理生理互联网!
早在19世纪,学者首次提出肾脏和心脏之间存在“微妙且高度相互依存的关系”。之后,心和肾的这种关系在血流动力学改变、神经体液活化、炎症以及氧化应激等多个方面不断更新[1]。
根据美国心脏协会(AHA)描述,这种关系被定义为心肾综合征(CRS),即心脏和肾脏其中一个器官的急性或慢性功能障碍,可能导致另一器官急性或慢性功能损害的临床综合征。
临床遇到CRS如何处置?首都医科大学附属安贞医院程虹教授在首届中国医药教育协会临床肾脏病学专委会年会上,进行了CRS实战经验分享。
心肾综合征的基础知识储备
在“实战推演”前,让我们先储备一些基础知识。
根据急性透析质量倡议(ADQI)工作组的分类,CRS被分为5型(图1),而各型CRS的主要病理特点如下:
1型CRS:低输出量导致肾脏血液灌注不足;
2型CRS:慢性炎症、氧化应激等引起的肾脏血液灌注降低;
3型CRS:严重水、电解质平衡紊乱、尿毒症和神经激素失调;
4型CRS:特异性心肌病、高容量负荷以及复杂机体内环境紊乱;
5型CRS:微循环功能障碍为主。
表1.心肾综合征的临床分型

临床上通常通过病史、体格检查、用药史、超声心动图、肾脏超声、容量评估以及最重要的心/肾生物标志物进行诊断,详细情况可见《70条推荐独家揭秘,我国最新心肾综合征指南来了!》。
在治疗上,目前没有任何特定疗法可降低CRS相关死亡率。容量管理和支持治疗仍然是CRS救治的主要手段。CRS的治疗应该在以下目标驱动下进行:
消除/减少诱发心功能或肾功能障碍的危险因素,积极治疗原发疾病;
改善心功能和肾功能,维持心血管状态稳定和肾脏血流灌注,减轻静脉淤血;
控制容量和炎症;
积极防治急慢性并发症;
减少复发风险;
提高患者生活质量,降低死亡风险。
病例实战演练时间来了
病例1
26岁男性,主因“尿检异常9年,胸闷气短1个月”。
▌病史资料
患者9年前双下肢水肿,血压 133/77 mmHg,尿蛋白2+,尿潜血-,24小时尿蛋白1.29g,SCr 74 μmol/L。肾穿刺病理示IgA肾病,小动脉未见明显病变。予贝那普利10 mg qd,半年后自行停药,未监测肾功能及血压。
2月前发现血压高,最高220/140 mmHg。口服苯磺酸氨氯地平5 mg bid及美托洛尔缓释片47.5 mg bid降压,自诉血压可控制在120/80 mmHg。
1月前受凉出现胸闷气短、双下肢水肿,BP 220/140 mmHg,尿蛋白4+,尿潜血-,24小时尿蛋白8g,SCr 434μmol/L,Hb 129g/L,BNP 1420 pg/mL,超声心动图示EF 27%,全心增大。胸部CT示胸腔积液心包积液、肺水肿。予利尿降压治疗,症状略好转。
复查SCr 416μmol/L,BNP 847pg/ml。近1月体重下降4kg。否认糖尿病、冠心病、脑血管病史。已戒烟1年,否认酗酒史。
▌体格检查
体温36.2℃,脉搏70次/分,呼吸18次/分,血压120/80mmHg身高180cm,体重120kg,BMI 37.0kg/m2,腰围120cm,全身皮肤未见皮疹,无水肿。双肺呼吸音清,未闻及干湿啰音及胸膜摩擦音。心尖搏动位于第5肋间左锁骨中线外0.5cm,叩诊心界向左扩大,心率70次/分,律齐,各瓣膜区未闻及杂音。双下肢无水肿。
▌实验室检查
血常规:WBC 9.13×109/L,Hb 129.0g/L,PLT 246×10/L。
尿常规:蛋白3+,RBC 4-8个/HP,WBC 0-3个/HP,管型未见。
24小时尿蛋白定量:3621.89mg/d。
肾功能:SCr 357.9μmol/L,BUN 10.79 mmol/L,eGFR 19.4 ml/min·1.73m2。禁水12h尿渗透压389 mOsm/kgHO,尿α1-MG 97.90mg/L。
生化:ALB 41.0g/L,UA 513.9μmol/L,TCHO 5.29mmol/L,LDH 176U/L,K 5.57mmol/L,总Ca 2.28mmo/L, iPTH 153.2pg/ml。
心脏损伤相关化验:hsTnl 20.3pg/ml,Myo 82.5ngml BNP 691.0pgml,NT-proBNP 3684.0pg/ml。
炎症相关指标:hsCRP 13.09mg/L,SF 220.0ngml。
免疫相关指标:均阴性。
▌辅助检查
腹部超声:左肾10.8cm×4.2cm×5.0cm,右肾11.2cm×4.6cm×4.9cm,肾实质回声增强。
超声心动图:LVEF 29%,室间隔厚度12mm,左室收末内径51mm,左室舒末内径60mm,左室壁运动普遍减低,左心增大,左室肥厚,心包积液(少量)。
心脏MRI:左心室正性重构,符合高血压心脏病改变,心功能减低,心包积液。
眼底检查:高血压视网膜病变2级(血压控制后检查结果)。
颈动脉超声:双侧颈动脉多发斑块,右侧颈内动脉起始中度狭窄。
颅脑MRI:双侧放射冠缺血,陈旧性脑梗死,左侧上颌窦囊肿。
冠状动脉钙化积分:58.8,轻度冠脉钙化。
▌病例讨论
该病例除了慢性肾功能不全的基础外,存在明确的高血压急性肾损伤。同时,综合分析病历资料,病例存在高血压心脏损伤引起的急性心脏损伤,为射血分数减少的心力衰竭(HFrEF)。综上所得,该病例可考虑为1、4或5型CRS。治疗原则上,应以血压控制达标为主,同时治疗慢性肾脏病(CKD)及心血管疾病(CVD)及其并发症以保护心肾。

图1.病例1治疗方案概括
治疗后,患者血压正常,无胸闷气短症状,hsCRP降至6.13mg/L,指标及检查变化分别如图2、表2所示。
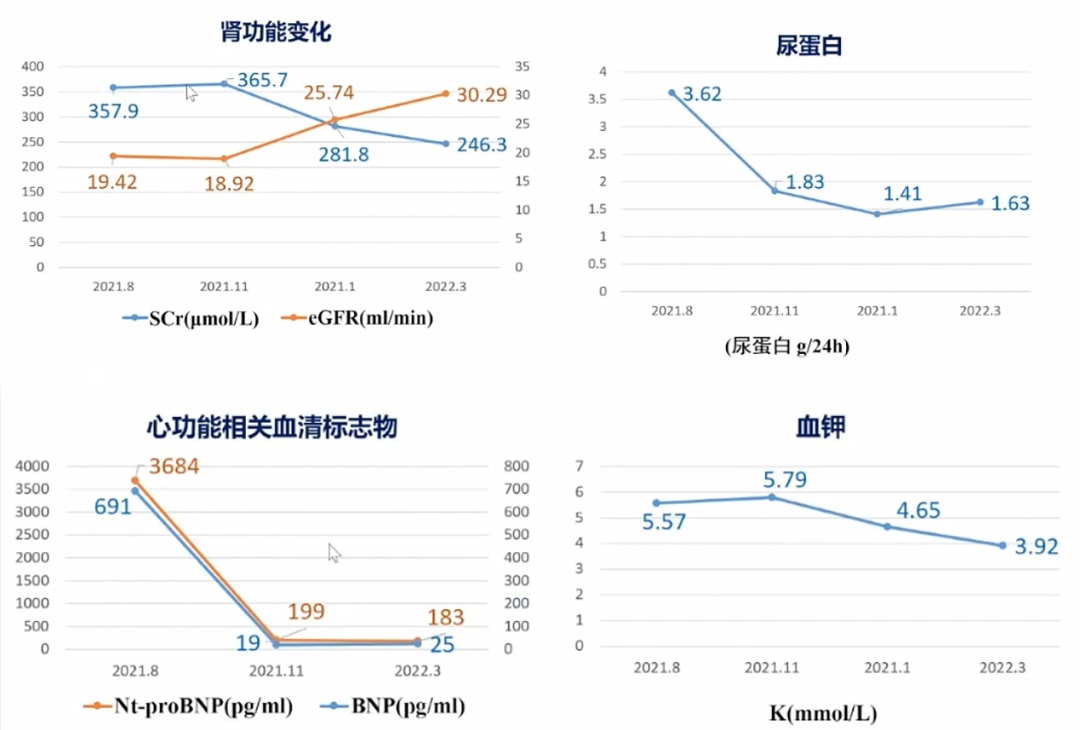
图2.治疗随访期间指标变化趋势(2021.8-2022.3)
表2.治疗随访期间超声心动图变化情况(2021.8-2022.3)
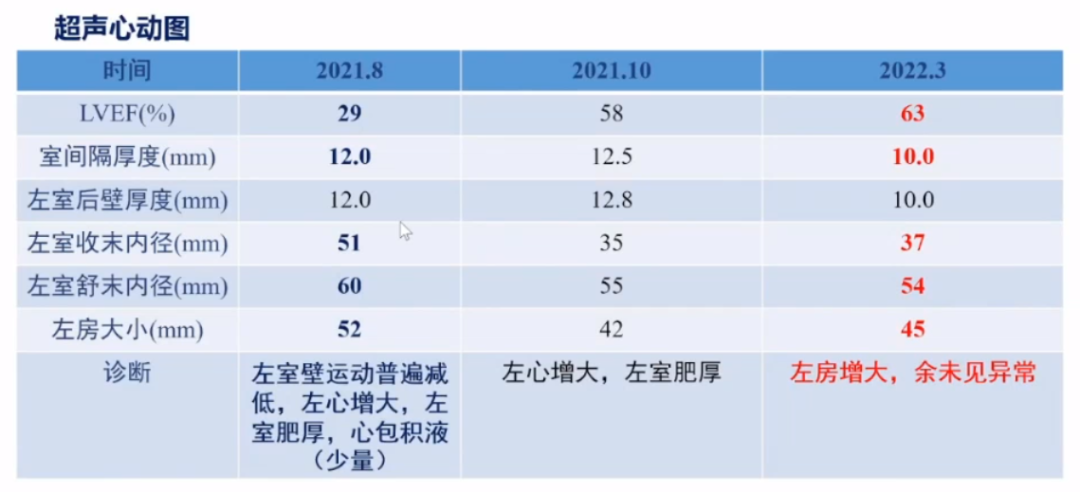
本例患者为HFrEF+CKD,根据改善全球肾脏病预后组织(KDIGO)的2019年共识[2],此类患者治疗选项包括肾移植、透析、连续肾脏替代治疗(CRRT)以及药物治疗(图3),而美国心脏病学会/美国心脏协会/美国心衰学会(AHA/ACC/HFSA)也于今年联合更新了心衰管理指南,CRS的治疗亦可参考此进行临床实践[3]。

图3.KDIGO推荐HFrEF合并CKD患者的治疗选项
病例2
49岁男性,主因“发现血压升高30余年,间断胸闷5天”
▌病史资料
患者自诉30余年前体检发现血压升高,具体不详,未诊治。6年前开始偶测血压150-160/100-110mmHg,无头晕、头痛,无视物模糊,未用药。
5天前无明显诱因出现胸闷、憋气,活动后加重,夜间可平卧入睡,无夜间阵发性呼吸困难,无浮肿,无尿量减少。
就诊于当地医院,测血压276/165mmHg,查Hb 81g/L,PLT 80×109L,尿常规示蛋白2+,离心尿沉渣镜检示红细胞3-6/HP,SCr 560 μmo/L,AIb 34.1g/L,cTnl 0.76ng/ml,CK-MB 3.98ng/ml,Myo 209ng/ml,BNP 766pg/ml,LDH 1003U/L。
予降压、利尿治疗,血压降至170-180/100-110mmHg,胸闷、憋气症状有所好转。夜尿增多2月余。吸烟15年,平均10支/日。有高血压家族史。
▌体格检查
体温36.8℃,脉搏104次/分,呼吸20次/分,血压168/93mmHg,BMI 25.5kg/m2,腰围88cm,全身皮肤未见皮疹,颜面部无水肿,双肺呼吸音清,未闻及干湿啰音,心率104次/分,心律齐,各瓣膜区未闻及杂音,双下肢无水肿。
▌实验室检查
血常规:WBC 5.6×109L,Hb 70g/L,PLT 107×109L。
外周血涂片:偶见破碎红细胞。
尿常规:蛋白+;尿沉渣镜检:RBC 3-7个HP,WBC 0-2个HP,颗粒管型0-2个/LP。
尿蛋白定量:1.0g/d。
肾功能:SCr 727.5μmol/L,BUN 31.5 nmol/L;尿α1-MG:86.9mg/L。
生化:ALB 32.8g/L,Glo 23.0g/L,UA 632.4μmol/L,Pi 1.92 mmol/L,iPTH 436.lpg/ml,LDH 701U/L。
心脏损伤相关指标:hsTnl 824.5pg/ml,CK-MB 1.4ng/ml,Myo 158.9 ng/ml,BNP 366pg/ml,NT-proBNP 17502pg/ml。
炎性相关指标:hsCRP 40.68mg/L,SF 755ng/ml。
免疫相关指标:均阴性。
▌辅助检查
眼底检查:视网膜散在出血及渗出,可见视乳头水肿。
腹部超声:左肾10.3cm×5.8cm×5.0cm,实质厚1.4cm,右肾10.8cm×4.7cm×4.1cm,实质厚1.2cm;双肾结构差。
超声心动图:LVEF 65%,左室肥厚,左房增大,节段性室壁运动异常。
颈动脉超声:双侧颈动脉斑块,左侧多发。
肾动脉超声:双肾动脉起始段未见明显狭窄。
肾上腺CT平扫:未见明显异常。
冠状动脉钙化积分:270.4,冠状动脉中度钙化。
腹X线:未见明显腹主动脉钙化。
▌病例讨论
本例高血压长期控制不佳,导致心脏、肾脏等靶器官受损,恶性高血压导致的急性心脏损伤和急性肾脏损伤持续“互相伤害“,导致病情不断恶性循环,导致舒张性心力衰竭(HFpEF),同时恶性高血压也引起了血栓性微血管病。
综合考虑,患者可为1、2、3或5型CRS,治疗同样当以血压控制达标为主,同时治疗CKD、CVD相关并发症从而保护心、肾等器官。

图4. 病例2治疗方案概括
治疗后,患者胸闷、憋气症状缓解,活动耐力增加,血压控制于130-140/70-80mmHg,hsCRP降至0.44mg/L,指标及检查变化分别如图5、6所示.
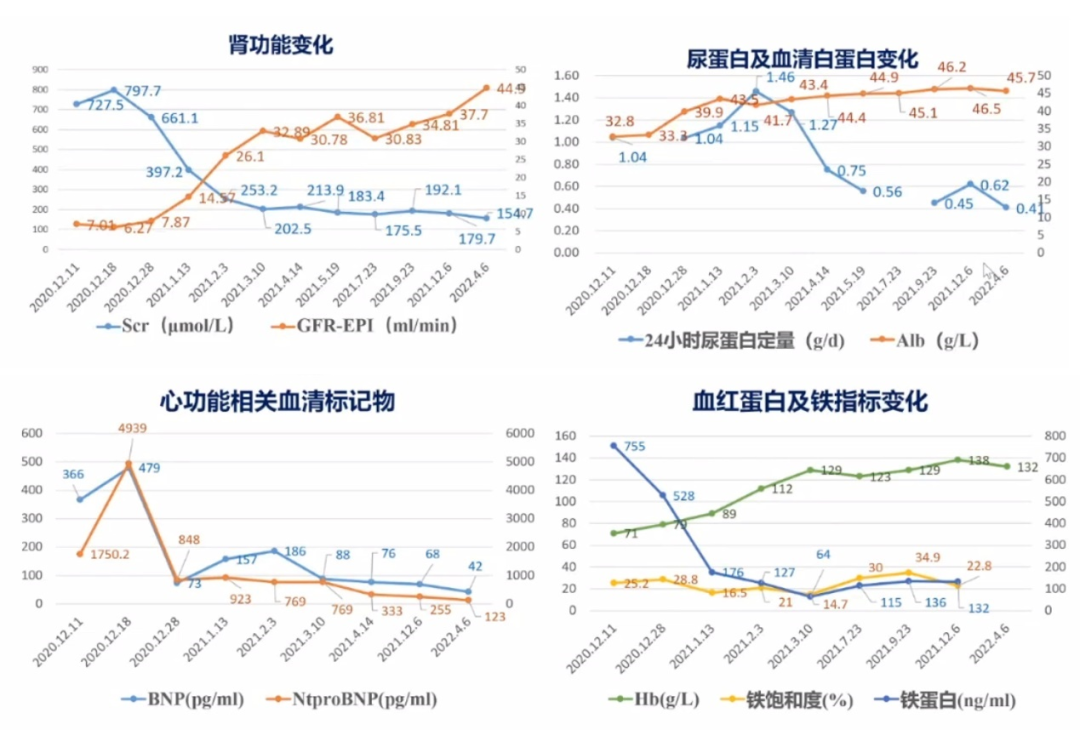
图5.治疗随访期间指标变化趋势(2020.12-2022.4)

图6.治疗随访期间指标变化情况(2020.12-2022.4)
本例患者为HFpEF+CKD,此类患者是高发病率和死亡率的高危群体,病因一般来自3方面:
并发症(糖尿病、血脂异常、高血压、睡眠呼吸暂停、肥胖);
血管疾病(动脉硬化、冠状动脉微血管功能不良、外周血管内皮功能不良);
肾脏因素(肾素-血管紧张素-醛固酮系统异常、高钙血症、高磷血症、贫血、尿毒症)。
同时,促炎环境、内皮功能障碍和全身充血是此类患者心肾功能障碍的病理生理学基础,与HFrEF相比更缺乏有效的“靶向“治疗[4,5]。
而安贞医院一项尚未发表的研究表明,CKD合并HFpEF患者的肾脏远期预后恶化风险显著增加,因此改善此类患者的肾脏预后十分必要。
上述2例患者有潜在冠脉病变的风险,尤其是冠脉CTA均显示有不同程度的钙化,须指出的是:冠心病的表型可随着肾功能的恶化而发生改变,传统观念往往倾向于凝视大动脉的典型阻塞性动脉粥样硬化病变,而小血管的动脉硬化即微血管疾病也应当引起重视。与普通人群相比,患有急性冠脉综合征的CKD患者临床表现往往更不典型,如:
以呼吸困难为主要症状,较少出现胸痛、臂痛或肩痛等典型症状;
急性心肌梗死更可能是非ST段抬高型心肌梗死(NSTEMI);
心肌纤维化通常见于肥厚的左心室。
这临床表型的变化与肾功能有关,且CKD分期越高,症状越不典型,其机制可能与动脉和瓣膜的内膜、内膜下和中膜钙化有关。因此,这类人群更应加强包括血运重建之外的控压、控糖、降脂及CKD相关并发症的治疗[6]。
总结
不难看出,临床严重CRS病例往往难以明确分型,心肾疾病交织糅合以及多种致病机制的参与导致病情复杂、临床治疗难度大、预后不佳,因此CRS的疾病管理需要多学科团队介入。
同时,无论是原发高血压或继发于肾脏疾病,恶性高血压往往可同时引发严重心、肾损害,其病变基础可能与补体系统异常活化所导致的血栓性微血管病(TMA)相关[7],其机理仍需深挖。
参考文献:
[1]Delgado-Valero B, Cachofeiro V, Martínez-Martínez E. Fibrosis, the bad actor in cardiorenal syndromes: mechanisms involved[J]. Cells, 2021, 10(7): 1824.
[2]House A A, Wanner C, Sarnak M J, et al. Heart failure in chronic kidney disease:conclusions from a Kidney Disease:Improving Global Outcomes (KDIGO) Controversies Conference[J]. Kidney international, 2019, 95(6):1304-1317.
[3]Heidenreich P A, Bozkurt B, Aguilar D, et al. 2022 AHA/ACC/HFSA guideline for the management of heart failure:a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines[J]. Journal of the American College of Cardiology, 2022, 79(17):e263-e421.
[4]Sacks D, Baxter B, Campbell B C V, et al. Multisociety consensus quality improvement revised consensus statement for endovascular therapy of acute ischemic stroke[J]. International journal of stroke, 2018, 13(6): 612-632.
[5]Ananthram M G, Gottlieb S S. Renal dysfunction and heart failure with preserved ejection fraction[J]. Heart Failure Clinics, 2021, 17(3): 357-367.
[6]Lopau K, Wanner C. Treatment rationale for coronary heart disease in advanced CKD[J]. Herz, 2021, 46(3): 221-227.
[7]徐潇漪,孙丽君,程虹,等. 补体活化在原发性恶性高血压合并严重心肾损伤中的作用[J]. 中华肾脏病杂志,2022,38(2):115-125. DOI:10.3760/cma.j.cn441217-20210319-00017.
更多精彩内容
| 留言与评论(共有 0 条评论) “” |