*仅供医学专业人士阅读参考
舒格利单抗是我国肺癌一线免疫治疗的优化选择!
“
晚期肺癌的治疗目标是最大限度地提高患者的长期生存获益,延缓疾病进展。随着免疫治疗在肺癌领域取得的突破性进展,尤其是GEMSTONE-302研究中,全球首个PD-L1抑制剂舒格利单抗联合化疗方案为患者带来的持久生存获益,这使其成为晚期非小细胞肺癌(NSCLC)的新治疗药物。
”2022年5月5日,在由辉瑞公司主办的“免疫云学院——2022肺癌免疫治疗MDT病例研讨会”上,河南省肿瘤医院带来两例晚期NSCLC诊疗病例精彩分享。“医学界”特邀该病例主治医生河南省肿瘤医院鲁俊锋医生详解其临床诊疗策略,河南省肿瘤医院赵艳秋教授进行精彩点评。
病例一分享
男,63岁,2019年4月就诊。主诉:咳嗽、咳痰伴痰中带血;吸烟史30余年,平均60支/天;饮酒史30年余,少量饮酒。外院CT示右肺上叶肿块影,考虑恶性;纵隔内、右肺门多发肿大的淋巴结,考虑转移可能。头部MRI及全身骨显像未见转移。
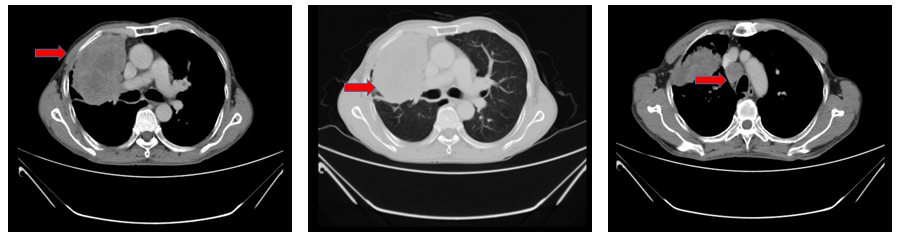
肺癌CT(基线)
外院支气管镜病理活检示鳞癌,本院会诊病理结果回示,免疫组化提示低分化鳞癌。
基因检测:肿瘤26基因检测结果回示,TP53基因突变;PD-L1(SP263)阳性肿瘤细胞比例为50%。
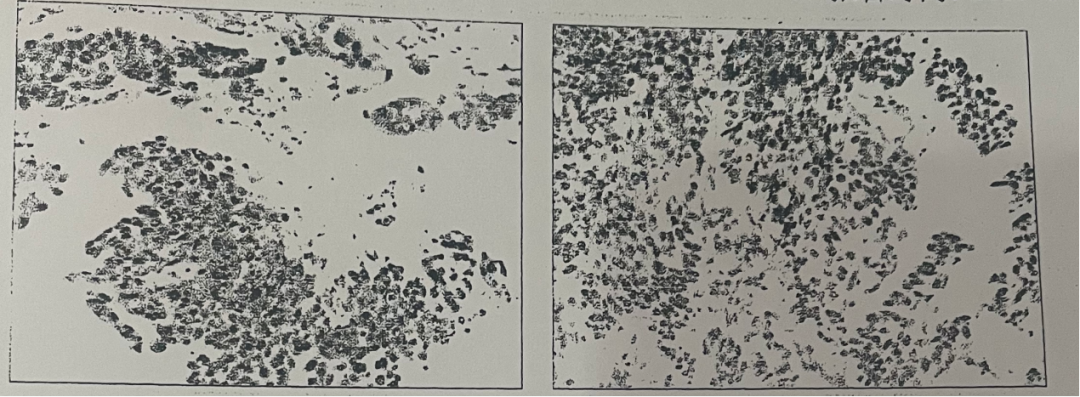
外院(右侧)支气管镜病理活检图示
临床诊断为:原发性右肺鳞癌并纵膈内淋巴结转移IIIB期(T4N2M0),EGFR/ALK/ROS1阴性,PD-L1表达为50%。
一线治疗
KEYNOTE-407研究结果证实[1],免疫联合卡铂和紫杉醇或白蛋白紫杉醇方案已成为驱动基因阴性晚期肺鳞癌的新的一线标准治疗。2022年《CSCO原发性肺癌诊疗指南》中[2],对于IV期驱动基因阴性、鳞癌的非小细胞肺癌患者,免疫单药(限PD-L1肿瘤细胞阳性比例分数(TPS)≥50%)以及免疫联合紫杉醇和铂类均为1A类证据。
2019年4月~7月,患者入组GEMSTONE-302研究,接受“紫杉醇+卡铂+舒格利单抗”方案进行6周期化疗(紫杉醇175mg/m2 d1 21d/周期,卡铂AUC=5,d1,21d/周期);
2019年8月~2021年11月,患者接受“舒格利单抗1200mg”维持治疗38周期,疗效评价为部分进展(PR);
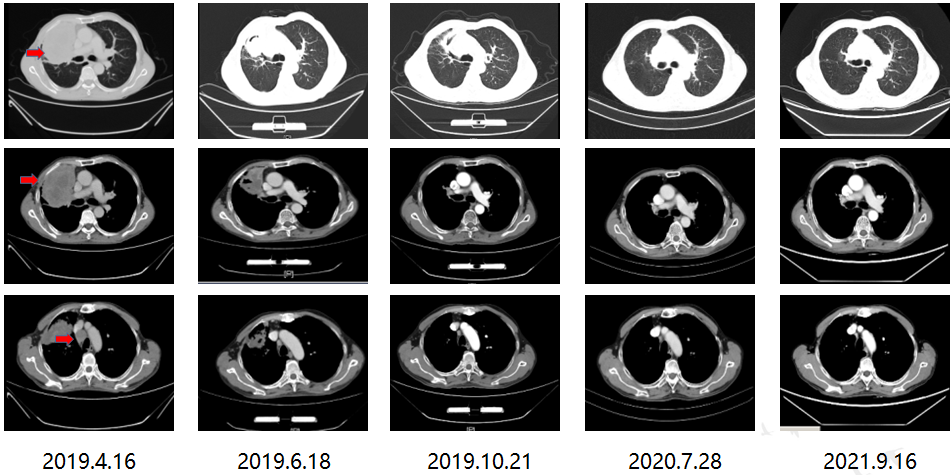
患者从接受舒格利单抗治疗至2021年9月的影像学对比
2021年12月患者进入延展期,继续给予“舒格利单抗1200mg”单药维持治疗至今。
病例二分享
男,58岁,2019年4月就诊。主诉:咳嗽、咳痰伴痰中带血;吸烟史30余年,平均1包/天;饮酒史30年余,3~4两/天。外院CT示左下肺门软组织肿块,考虑肺癌可能;左侧锁骨上、纵隔内及左肺门多发肿大的淋巴结,考虑转移。头部MRI及全身骨显像未见转移。
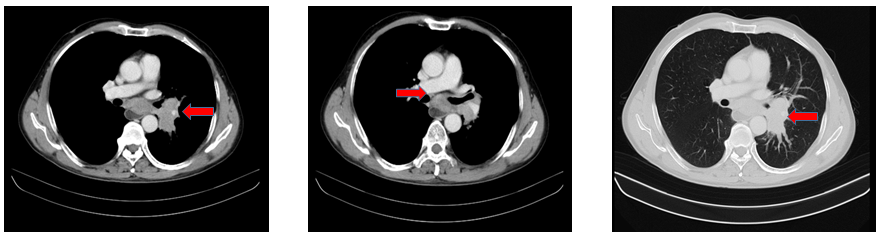
肺癌CT(基线)
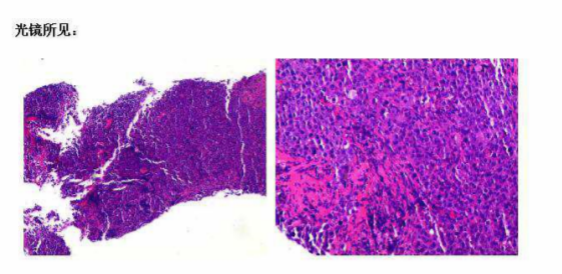
病理检测结果
穿刺活检病理:(左肺)非小细胞低分化鳞癌。
免疫组化示:CK(+)、Vim(-)、P40(+)、PDL-1(TPS=9%)、Ki67(约60%)。
基因检测:肿瘤26基因检测结果回示,TP53基因突变。
临床诊断为:原发性左肺鳞状细胞癌并左侧锁骨上、纵膈内及肺门淋巴结转移(T3N3M0 IIIC),EGFR/ALK/ROS1阴性,PD-L1表达为9%。
一线治疗
2019年4月~7月,患者入组GEMSTONE-302研究,接受 “紫杉醇+卡铂+舒格利单抗”方案进行5周期化疗;
2019年8月~2021年11月,患者接受“舒格利单抗1200mg”维持治疗38周期,疗效评价为PR;
2021年12月患者进入延展期,继续给予“舒格利单抗1200mg”单药维持治疗至今。
专家点评
赵艳秋教授针对上述两例一线行舒格利单抗联合治疗获得长期肿瘤缓解,且目前仍在持续获得缓解的患者的治疗策略进行深入分析与探讨。
舒格利单抗为肺鳞癌患者的更优选择
肺癌居于我国男性及女性癌症相关死亡原因的首位,大多数患者在确诊时已属晚期,5年生存率仅为18%[3]。在所有肺癌患者中,NSCLC患者约占80%-85%,根据组织学类型,其可分为腺癌(约占40%),鳞状细胞癌(21%-30%)和大细胞癌(10%)等亚型[4]。与肺腺癌相比,肺鳞癌由于肿瘤的高度异质性及突变负荷高,使得在临床上难以找到明确的靶点而进行治疗。既往对于晚期肺鳞癌的治疗,含铂双药化疗一直是一线标准方案,然而由于化疗毒性的限制,化疗的联合已进入疗效瓶颈。随着不同免疫制剂联合化疗方案一线治疗晚期肺鳞癌适应证的不断获批,免疫治疗方案大幅拓展晚期肺鳞癌患者一线选择。
其中,GEMSTONE-302研究中全球首个抗PD-L1单抗联合化疗作为一线治疗,可同时用于IV期鳞状和非鳞状NSCLC患者,在改变中国肺癌治疗手段的同时,极大地延长患者的生存时间,改善患者的预后,将成为国内晚期肺鳞癌患者更好的一线治疗选择。
安全性良好,舒格利单抗联合化疗方案获2022CSCO指南I级推荐
GEMSTONE-302研究显示,无论PD-L1表达状态如何,舒格利单抗均充分体现了免疫治疗长效获益的特点,这在两例临床病例汇报中已体现得淋漓尽致:两例患者入组GEMSTONE-302临床研究后,一线治疗过程中接受舒格利单抗+紫杉醇+卡铂联合治疗,后序贯舒格利单抗单药维持治疗38周,进入延展期后给予舒格利单抗单药治疗至今。而且,两例患者在治疗过程中无特殊不良反应,耐受性良好,未出现任何免疫治疗相关不良反应。
据悉,GEMSTONE-302研究结果显示[5],舒格利单抗联合治疗组与安慰剂组的PFS分别为9.0个月和4.9个月(HR=0.48,P<0.0001),显著延长4.1个月,疾病进展或死亡风险显著降低52%。2021年世界肺癌大会(WCLC)公布的PFS亚组分析数据显示[6],舒格利单抗联合化疗对肺鳞癌人群的诊疗优势更为明显,肺鳞癌组患者PFS分别为8.3个月和4.8个月(HR=0.34),可以显著降低疾病进展与死亡风险达66%;对比非鳞癌组患者,其HR值为0.59。
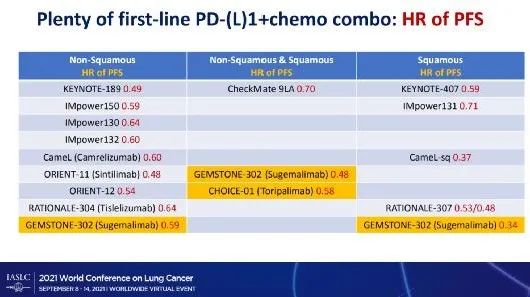
2021 WCLC截图(非头对头对比研究,勿直接对比解读)
安全性分析结果显示[6],舒格利单抗组≥3级不良事件(AE)发生率与单纯化疗组相当,绝对值仅高2.5%(64.1% vs. 61.6%);≥3级免疫相关AE发生率仅4.1%(4.1% vs. 0),≥3级免疫相关性肺炎发生率仅0.9%,这充分证明了舒格利单抗具有较好的安全性优势。对此,赵艳秋教授表示,较低的间质性肺炎和肝毒性发生率是舒格利单抗的一大优势。
基于舒格利单抗卓越的疗效和安全性,在2022年的最新版中国临床肿瘤学会(CSCO)指南中[2],已新增GEMSTONE-302模式作为IV期无驱动基因、鳞癌NSCLC一线治疗的I级推荐。
免疫新时代,免疫治疗生物标志物的预测及精准获益仍需不断探索和前行
舒格利单抗作为我国首个获批的全人源全长抗PD-L1抑制剂,其通过对抗体Fc段改造,增强抗肿瘤活性增强,同时降低免疫不良反应。对于驱动基因阴性晚期NSCLC的治疗,免疫治疗联合化疗已经成为当前新的一线治疗标准,为NSCLC患者带来长生存获益。但同时需要注意的是,尽管免疫治疗对于既往化疗具有更优的总生存期(OS)与PFS数据,但其也存在局限性,如患者的5年OS并未提高良多,治疗相关不良反应的个体化控制,免疫生物标志物对于临床预后,免疫获益人群的精准分层等,仍需进一步展开相关研究与探索,以期为患者带来更精准的获益与更优的治疗选择。

择捷美产品说明书
病例声明:会议中涉及的病例分享和讨论仅为教育和交流用途,不涉及会诊和干预诊疗。相关诊疗决定由医生根据患者情况独立作出。
专家简介
鲁俊锋 住院医师
河南省肿瘤医院 呼吸内一科
硕士毕业于郑州大学 临床医学七年制
博士毕业于中山大学
专业方向:晚期肺癌的综合治疗、肿瘤的基础与临床研究
成果:发表SCI 12篇,其中第一作者及共同第一作者SCI 5篇(单篇影响因子最高9.3分),主持国家自然青年科学基金一项
专家简介

赵艳秋 教授
河南省肿瘤医院内科副主任,主任医师
呼吸内科一病区主任
河南省肿瘤医院肺癌、食管癌首席专家组成员
中国抗癌协会食管癌专业委员会委员
河南省抗癌协会药物临床研究专业委员会副主委
河南省抗癌协会肿瘤分子医学专业委员会副主委
审批码:PP-CEJ-CHN-0420
有效期:2023-7-28
参考文献:
[1].Paz-Ares L,Luft A,Vicente D,et al.Pembrolizumab plus chemotherapy for squamous non-small-cell lung cancer[J].N Engl J Med 2018;379:2040-51.
[2].《2022CSCO非小细胞肺癌诊疗指南》.
[3]. Siegel RL, Miller KD, Jemal A. Cancer statistics, 2015. CA Cancer J Clin, 2015, 65(1): 5-29.
[4].任红亮, 等. 探讨PET/CT原发灶SUVmax在肺鳞癌患者术后预后中的意义及与临床病理特征的关系[J]. 中国肺癌杂志, 2016,19(4):192-199.
[5].Zhou CC, et al. Sugemalimab versus placebo, in combination with platinum-based chemotherapy, as first-line treatment of metastatic non-small-cell lung cancer (GEMSTONE-302): interim and final analyses of a double-blind, randomised, phase 3 clinical trial. Lancet Oncol. 2022 Feb;23(2):220-233.
[6]. Keunchil Park, MD, PhD. Building on the Past: What Will Be the Next Immunotherapy Combination? Presented at: 2021 World Conference on Lung Cancer; September 8-14, 2021. Virtual. Abstract MA13.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |