*仅供医学专业人士阅读参考

免疫治疗时代给患者带来了更多的治疗选择,也给临床实践拓宽了探索之路。
肺癌是中国最常见的癌症。其居高不下的发病率与死亡率对肺癌治疗提出了高要求,新的诊断与分型方法、治疗药物与手段层出不穷,为肺癌综合管理策略提供了丰富的治疗选择。
长期生存作为肺癌管理的重要目标,一直是各肺癌MDT临床研究团队致力攻克的难题。
2022年7月26日,由南京大学医学院附属金陵医院宋勇教授MDT团队主持,来自中国科学技术大学附属第一医院的操乐杰教授MDT团队、来自陆军军医大学附属第一医院的周向东教授MDT团队和来自上海交通大学附属瑞金医院的项秩教授MDT团队各自分享了各自管理过的综合治疗下实现长期生存或理想疗效的病例,为精准治疗在肺癌管理中的应用提供了重要启示。
该病例分享来自操乐杰教授MDT团队,由冷再君医生汇报的“一例生存期超过5年的晚期NSCLC病例”。
基本信息
66岁女性,因咳嗽两月余于2016年4月入院。既往无吸烟史。体格检查无特殊。
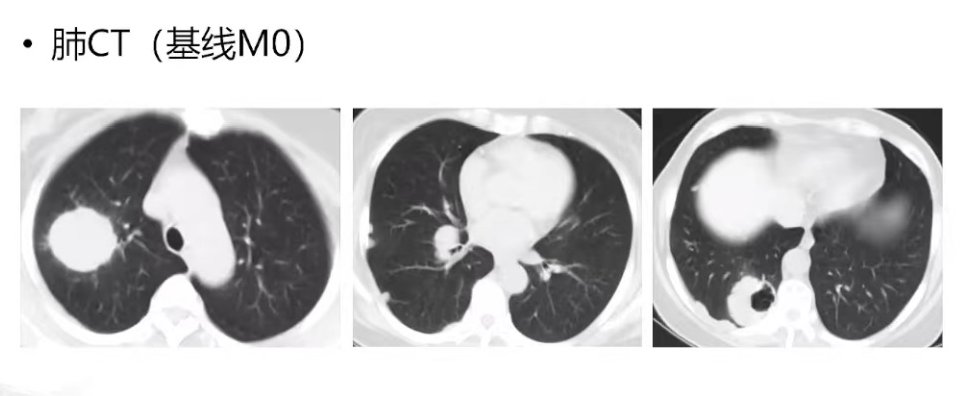
影像学资料:
基线M0:右肺多个病灶,右肺上叶肿块影,伴小毛刺和浅分叶。右侧肺门淋巴结肿大,右侧胸膜下多发结节,右侧基底段结节伴空洞形成。
经皮肺穿刺活检+病理:低分化癌,免疫组化标记结果符合腺癌。免疫组化:CK7+,Napsin-A+,TTF-1+,CK5-,P63-,P40-,Syn-,CgA-,CD56-,Ki-67+约10%。基因检测显示EGFR-19缺失阳性突变。
诊断:右肺腺癌(T4N1M1a,IVA期,EGFR-EX19del)
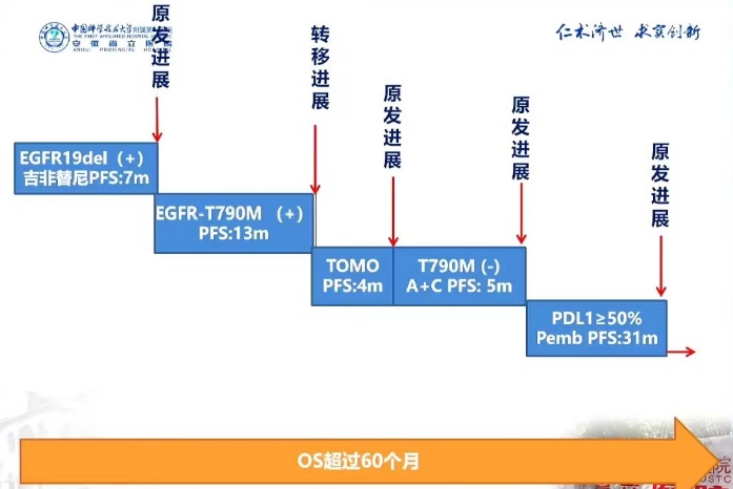
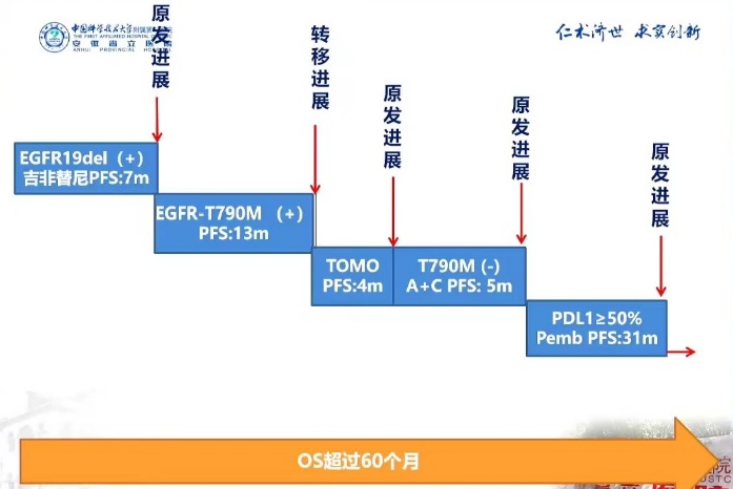
治疗过程:五次进展,五种方案
2009年的IPASS研究是肺癌靶向治疗的一座里程碑,此研究提出,对于EGFR突变阳性的患者,对比含铂双药化疗,使用EGFR-TKI可以实现明显的生存获益,无进展生存期(PFS)明显延长。美国国家综合癌症网络(NCCN)指南推荐对于EGFR阳性突变的NSCLC患者使用EGFR-TKI可作为一线治疗选择。
因此,患者接受吉非替尼0.25g Qd。
患者使用吉非替尼第3个月,复查肺部CT发现,右肺上、下叶病灶明显缩小,右侧肺门淋巴结缩小,右侧胸膜结节消失,疗效评估为部分缓解(PR)。
然而,在第7个月时,复查肺部CT时发现患者右肺上叶及基底段病灶增大,右侧胸膜下出现新发结节,病情出现原发进展。
此时,患者使用一代EGFR-TKI吉非替尼7个月后发生耐药。
针对这种情况,2019年的NCCN指南中推荐,对于一代或二代EGFR-TKI耐药的患者进行T790M基因检测,检测阳性的患者,可更换三代EGFR-TKI奥希替尼口服。
2016年的AURA3研究也指出,对于一代EGFR-TKI耐药的患者,对比含铂双药化疗,口服奥希替尼可延长PFS期(分别为4.4个月和10.1个月)。以上研究均提示,二次活检完善基因检测是十分必要的。
在第7个月,患者完善了二次活检并基因检测,结果为EGFR-EX19del(+),T790M(+),因此,医生为该患者更换了二线治疗方案奥希替尼80mg Qd口服。
第20个月时,复查肺部CT显示右上肺、基底段病灶缩小,右侧胸膜下结节减少,疗效评估为PR。
然而,患者随后出现了头痛、头晕、呕吐的症状,完善头部MRI显示脑部转移病灶,出现转移进展。奥希替尼为患者带来了13个月的PFS。
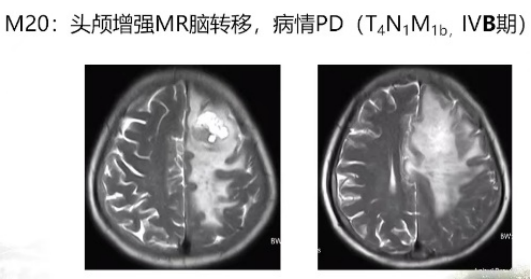
下一步根据2019 NCCN指南,对于奥希替尼耐药的脑转移NSCLC患者,可选择局部治疗。
因此,医生在原有奥希替尼80mg Qd口服的基础上,给予患者头颅TOMO放疗(95%PGTV 6000cgv/20f/40w)。头部症状好转,复查头部MRI发现脑转移病灶减小,脑水肿消退。
M24时复查肺部CT发现右肺下叶原发病灶再次出现原发进展,奥希替尼+TOMO为患者实现了4个月的PFS。
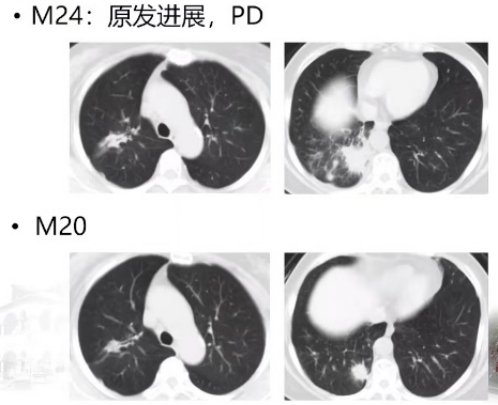
针对三代EGFR-TKI耐药的处理,首先需要明确耐药机制,可分为EGFR依赖型和非EGFR依赖型。对于EGFR依赖型,根据C797S和T790M基因检测的结果,选择一代到三代EGFR-TKI。对于非EGFR依赖型,即耐药机制涉及其他旁路如MET、HER2等,可联合其他靶向治疗。若发生小细胞转化(SCLC),可选择EP方案。因此,明确耐药机制对于指导下一步化疗十分关键。
在第24个月时,患者行第三次穿刺活检+mNGS,检测结果显示EGFR-19del,T790M(-)。
根据2019 NCCN指南,系统性治疗后进展的NSCLC患者,可考虑使用免疫检查点抑制剂或系统性化疗如多西他赛、吉西他滨等。而EGFR突变阳性作为免疫治疗的反指征,可能会导致疾病超进展。
因此,医生暂时没有考虑免疫治疗,而是为患者更换了三线治疗方案:培美曲塞0.8g+贝伐珠单抗400mg Q21d×4周期+贝伐珠单抗400mg×1周期的三线治疗方案。
第24个月,肺部CT显示右肺上叶病灶稳定,右下叶病灶稍缩小,疗效欠理想。
第29个月时,患者右下叶基底段病灶增大,出现了第三次原发进展,此时查头部MRI显示头部转移灶控制尚可。三线治疗方案的使用为患者实现了5个月的PFS。
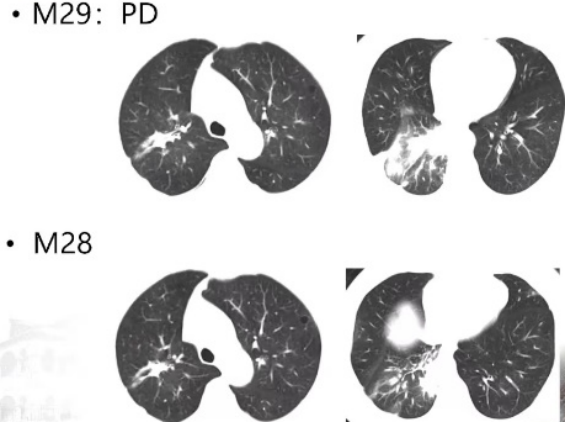
对于三线治疗依旧发生了耐药的患者,医生开始考虑应用免疫治疗的可能性。
SITC推荐,EGFR/ALK/ROS1敏感突变者,一线TKI治疗耐药后,二线若伴PD-L1≥50%高表达,可考虑使用帕博利珠单抗。2018年的NCCN指南也推荐NSCLC患者进行PD-L1检测,并将后续人群分为三大类:基因突变靶向治疗群、PD-L1≥50%免疫治疗群和靶向、免疫均不受益的传统放化疗治疗群。KEYNTE024研究表明,帕博利珠单抗一线治疗PD-L1 TPS≥50%的NSCLC患者显示出生存获益。Impower150研究是首个显示经治疗EGFR突变阳性患者能获益于免疫检查点抑制剂的III期临床试验。
在M29时,患者接受了第四次活检+基因检测,结果显示PD-L1:80%。在排除免疫治疗禁忌、并获得充分知情同意的前提下,医生为患者调整了四线治疗方案:帕博利珠单抗200mg Q3W。
M30、M34、M36、M41、M44时评估治疗效果,肺部CT显示右上叶、基底部病灶缩小,达到维持性的PR。
M48时,患者因“突发言语不清,右下肢肢体无力”于2020年4月入住神经内科,怀疑脑部转移灶进展,予完善肺部CT和头颅MRI检查,头MR提示右侧额叶多发急性期脑梗塞,肺部CT展示维持性PR。神经内科住院时针对脑梗塞进行对症治疗,并继续予以帕博利珠单抗维持治疗。
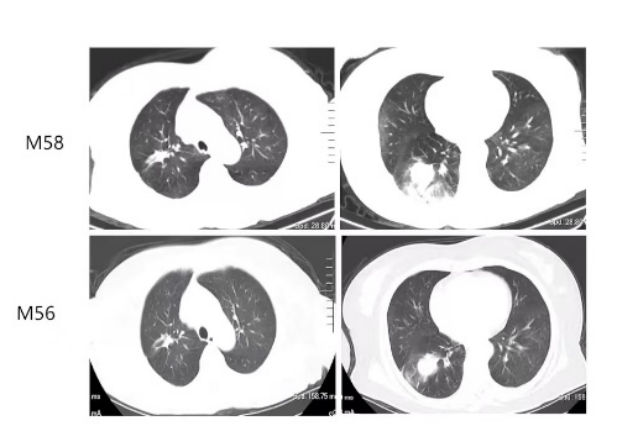
M56和M58复查肺部CT,右肺下叶病灶再次增大,考虑出现了第四次原发进展。帕博利珠单抗为患者带来了31个月的PFS。
免疫治疗不良反应(irAE):
甲状腺功能减退+糖尿病
在使用帕博利珠单抗的过程中,患者出现了一些以内分泌系统表现为主的不良反应,包括甲减、糖尿病,分别给予了左甲状腺素片和胰岛素治疗。
作为常见的免疫治疗相关不良反应(发生率分别为40%和0.2%~0.9%),一般推荐对甲减和糖尿病患者给予对症治疗,而不需要停止免疫治疗。
专家点评
回顾完整治疗经过,患者总生存(OS)期超过了60个月,主要的PFS获益于免疫治疗。
针对这个病例,冷再君医生提出,EGFR敏感突变患者也是免疫治疗的潜在获益人群,但在用药期间需检测血糖、甲状腺功能。而该患者可长期生存的原因是多方面的,除了规范治疗、全程管理,还得益于医患信任与配合。
中国科学技术大学附属第一医院肿瘤放疗科的钱东教授从放疗角度对病例进行了点评,他指出:“在靶向治疗时代,在疾病出现局部的寡进展阶段时及时给予局部治疗,可延缓患者进入系统进展阶段,给予更多的治疗选择,为患者带来更多获益。”钱东教授同时提出了一个问题,即在最后一次右肺下叶基底段的局部进展阶段是否可以考虑给予局部放疗以尝试增加免疫治疗获益,尽管一些研究发现局部低剂量放疗可激活免疫而增强免疫治疗效果,但仍有待高级别证据的支持。内科免疫治疗与放疗的配合以增强免疫治疗的疗效将成为未来肿瘤治疗的发展方向之一。而针对操乐杰教授提出的“TOMO治疗是否会引起或加重脑梗塞或是否有远期影响”这一问题,钱东教授给出了以下回答:“长期放疗可引起血管闭塞,大剂量放疗也可引起脑坏死,很难与脑梗死鉴别。因此,放疗应进一步提高局部定位精确性,以避免或减少脑坏死的发生。”
中国科学技术大学附属第一医院肺及纵隔外科的解明然教授对该患者的规范程度及治疗效果给予了充分肯定,并指出了肺癌患者内科化疗+免疫治疗联合外科治疗的良好前景,值得进一步的探索与突破。
操乐杰教授对这一病例总结指出:“首先,对于该患者的分次诊断和及时的治疗方案调整获得了良好效果,这提示对于NSCLC患者而言,如何平衡靶向治疗与免疫治疗值得进一步探索。其次,要总结经验教训,预防肿瘤患者脑梗死的发生。”
陆军军医大学附属第一医院周向东教授对此病例点评指出:“该病例管理十分规范,但在维持治疗阶段,出现病灶控制不佳时,就可以进行活检以早期掌握病情变化情况。免疫治疗阶段可多次进行全身评估,包括凝血功能以判断是否需要抗凝治疗。”
南京大学医学院附属金陵医院宋勇教授团队的专家分别从多个角度对此病例进行了点评。病理科沈勤教授指出:“此患者在全程诊治过程中,良好地应用了病理诊断的手段。在首次病理诊断时,低分化腺癌是多种基因突变共存的高危因素,鉴于当时的技术限制,未能进行全景基因突变的检测,可能是患者在7个月时出现疾病进展的原因之一。”放射科朱锡旭教授指出:“首先,患者接受头部放疗后,头部转移灶长期未进展,表明患者对放疗敏感。其次,患者复发多为肺部的原位复发,而少累及其他部位。因此,在靶向治疗或免疫治疗出现反复复发时,可以考虑在肺部使用局部放疗以增强治疗效果。”
长按识别海报下方二维码
| 留言与评论(共有 0 条评论) “” |