*仅供医学专业人士阅读参考

直击WCLC,医学界带你看NSCLC一线治疗新进展!
肺癌靶向、免疫新药的研发呈现井喷式发展,因此,如何让NSCLC患者在一线治疗时即实现获益最大化,进而让患者实现长期生存,成为了学界研究的焦点。在2022年8月6日至9日由国际肺癌研究协会(IASLC)在奥地利维也纳主办2022年世界肺癌大会(WCLC)上,就展现了相应的研究成果,让我们一睹为快。
Avelumab vs Chemotherapy for First-line Treatment of Advanced PD-L1+NSCLC:Primary Analysis from JAVELIN Lung 100.
摘要:OA15.03
JAVELIN Lung 100:对比Avelumab和化疗一线治疗NSCLC疗效
Avelumab是抗PD-L1的单抗,在NSCLC的治疗中显示了抗肿瘤的活性以及可接受的安全性。M.Reck教授团队进行了开放标签、多中心的Ⅲ期的JAVELIN LUNG 100研究,以期明确Avelumab单药(两个剂量方案)相比以铂为基础的双药化疗治疗PD-L1阳性晚期NSCLC的疗效和安全性[1]。

2022WCLC摘要截图
研究者一共纳入了1214例PD-L1阳性(PD-L1表达≥1%)以及EGFR/ALK为野生型的未经治疗的转移或复发(M/R)的Ⅳ期NSCLC患者,患者在最开始按照1:1的比例被随机分入Avelumab 10mg/kg每2周一次(Q2W)以及含铂双药化疗组[每3周一次(Q3W)],按照病理进行分层。随后,根据药代动力学和暴露分析对于方案进行修订后,患者按照1:2:2的比例随机分入Avelumab(10mg/kg)Q2W组、含铂双药化疗Q3W组以及Avelumab QW组(10mg/kg QW实行12周之后,采取10mg/kg Q2W方案给药),此时按照组织学和PD-L1表达(高≥80%;中度≥50%;任何≥1%)分层。研究主要终点是经独立审查委员会(IRC)。
评估的PD-L1高表达晚期NSCLC患者的总生存期(OS)和无疾病进展生存期(PFS),结果显示:
患者分布显示Avelumab Q2W组为366例,含铂双药化疗组为526例,Avelumab QW组为322例,截至2021年10月,随访时间已经超过41个月;
各个Avelumab组和含铂双药化疗组之间,并未观察到OS和PFS的显著差异(图1);
在PD-L1高表达的患者中,Avelumab Q2W组、Avelumab QW组以及含铂双药化疗组在研究结束之后,接受抗PD-1/L1单抗治疗的比例分别为5.3%、20.2%和30.6%;
Avelumab Q2W组、Avelumab QW组以及含铂双药化疗组出现治疗相关不良反应(TEAEs)的比例分别为95.8%、96.6%和96.8%,≥3级的不良反应比例分别为60.1%、56.9%和64.8%;
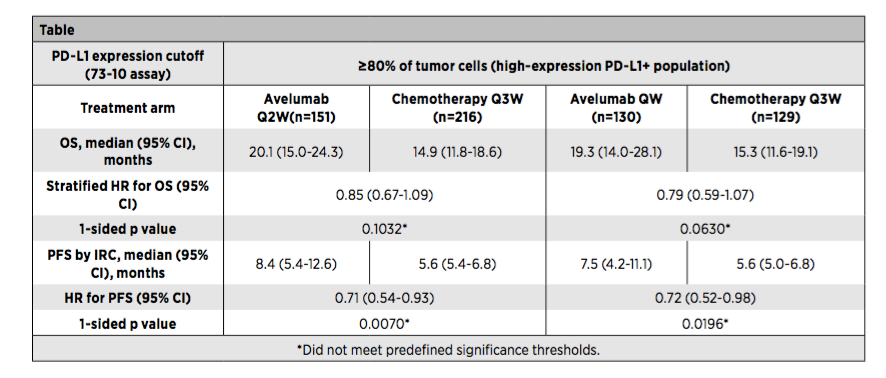
图1:JAVELIN LUNG 100研究PD-L1高表达人群疗效结果
总之,经IRC评估JAVELIN LUNG 100研究并未显示Avelumab(Q2W或Q1W)相比含铂双药化疗在PD-L1高表达NSCLC患者中具有OS和PFS优势。安全性结果与既往研究结果一致。
MA13.07 TROPION-Lung02:Initial Results for Datopotamab Deruxtecan Plus Pembrolizumab and Platinum Chemotherapy in Advanced NSCLC
ADC药物Datopotamab Deruxtecan联合免疫检查点抑制剂+化疗治疗晚期NSCLC颇具前景
绝大多数NSCLC患者在前线治疗开始8~10个月之后,就会出现复发,因此,亟需新型治疗方式以应对该治疗需求。Datopotamab Deruxtecan(Dato-DXd)是TROP2的抗体偶联药物(ADC),单药治疗在复发/难治(R/R)晚期/转移性NSCLC治疗中显示了令人鼓舞的活性和可管理的安全性[NCT03401385,6mg/kg治疗时,客观缓解率(ORR)为28%,缓解持续时间(DoR)为10.5个月]。此外,在临床前研究显示,Dato-DXd联合PD-1单抗相比两者单独使用都更具缩瘤效应,因此,B.Levy教授团队发起了全球、Ⅰb期、剂量递增和扩增的TROPION-Lung02研究,以明确Dato-DXd联合帕博利珠单抗±化疗在NSCLC治疗中的初期疗效和安全性。

2022WCLC摘要截图
研究者一共设置了6个队列,每个队列约为20例患者(表1),除非另有说明,否则扩展队列中的患者均为既往未接受过治疗的晚期/转移性NSCLC患者。研究的主要目标是评估耐受性和安全性,次要目标是评估疗效、药代动力学和抗药物抗体。截至2022年1月,一共有60例患者进行了治疗,患者的中位年龄为64岁,35%的患者PD-L1表达<1%,而PD-L1表达为1%~49%以及PD-L1表达≥50%的患者比例均为25%,剩余15%的患者PD-L1表达状态未知。研究结果显示:
中位治疗持续时间为2.7个月,当前仍然有67%的患者正在接受治疗;
在安全性方面,10%的患者因不良反应而停止治疗,20%的患者在使用Dato-DXd时进行了减量,43%的患者出现了≥3级的不良反应,最常见的任何级别的不良反应是口腔炎(42%)、恶心(38%)和疲劳(27%),未发现治疗相关间质性肺病的发生;
所有联合治疗组均被认为可耐受治疗,且可以转为剂量扩展队列;
在跨队列的可评估治疗反应的46例患者中,ORR为39%[9例为部分缓解(PR),9例正在转变为PR,疗效待确认],疾病控制率(DCR)为82.6%;
在16例可评估疗效的一线治疗的患者中,ORR为69%(5例已经确认为PR,6例为正在转变为PR,疗效待确认),DCR为100%。
表1:6个队列的治疗组合和方案
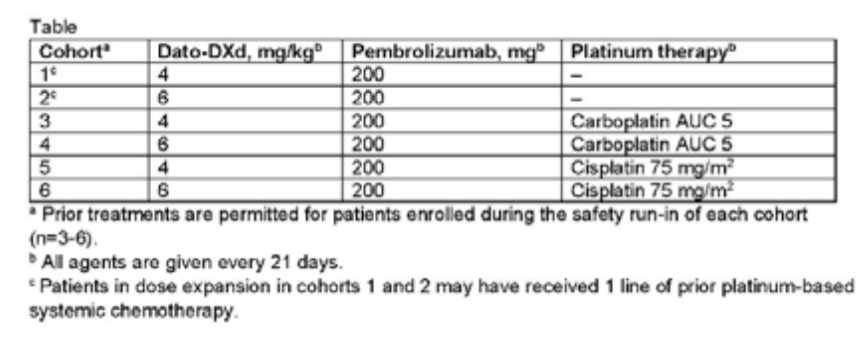
总之,在NSCLC前线和或复发/难治的后线治疗之中,Dato-DXd联合帕博利珠单抗±铂类化疗显示了可耐受的安全性和显著的抗肿瘤活性。据研究者所知,该研究是第一个报道在NSCLC患者中,使用Dato-DXd联合帕博利珠单抗±铂类化疗治疗的研究。
参考文献:
[1]M.Reck,et al.OA15.03.2022WCLC.
[2]B.Levy,et al.MA13.07.2022WCLC.
本文首发:医学界肿瘤频道
本文作者:放瘤娃
责任编辑:Sweet
| 留言与评论(共有 0 条评论) “” |