*仅供医学专业人士阅读参考

肺癌精彩病例分享,一键查收!
本病例为53岁女性晚期右肺腺癌患者,同时伴有右肺门、纵隔、双锁骨区淋巴结转移,骨、肝、脑多发转移,并右肺阻塞性肺炎及右侧胸腔积液。初次诊断为EGFR 19del突变,一线经埃克替尼治疗后耐药,无进展生存期(PFS)为11个月。二线治疗改为奥希替尼靶向治疗,11个月后出现疾病进展(PD)。2020年11月至2021年9月,患者三至六线分别接受标准化疗、抗血管生成药物等治疗方案,期间配合脑转移灶以及锥体转移灶放疗,但疗效不佳,疾病均快速出现进展。
2021年10月,患者进行采用液滴式数字PCR(ddPCR)基因检测,结果显示为MET扩增,七线接受赛沃替尼联合奥希替尼治疗,肿瘤疾病稳定(SD),PFS已达到9个月,至今仍在接受治疗并且积极随访中。该病例由福建省肿瘤医院黄章洲教授提供,并邀请福建省肿瘤医院庄武教授进行点评。
病例简介
基本情况:患者女,53岁,因“反复咳嗽、胸闷20余天”于2018年11月2日首次入院。
既往史:乙肝表面抗原携带者。
现病史:20余天前无明显无吸烟史。诱因出现阵发性咳嗽、咳少量白色粘痰,就诊于三明市第二医院。
胸部+鼻窦CT:右侧额叶占位,建议MRI,右肺门占位可能,纵膈多发淋巴结肿大,右肺炎症,右侧胸腔积液,肝内多发占位。
胸部+腹部CT:右肺中央型肺癌纵隔、双锁骨区、右肺门淋巴结转移并右肺阻塞性肺炎及右侧胸腔积液;肝内多发转移瘤。
头颅MRI:颅内多发转移。
全身骨ECT:胸骨柄、右侧第4肋骨放射性异常分布,考虑骨转移。
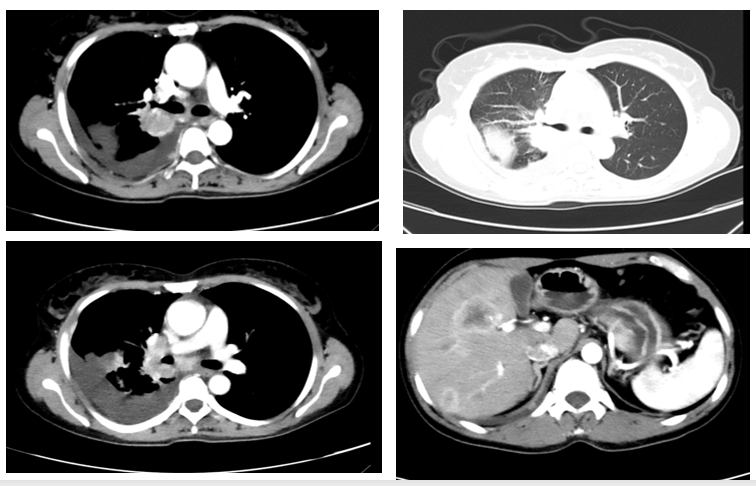
患者基线胸部+腹部CT
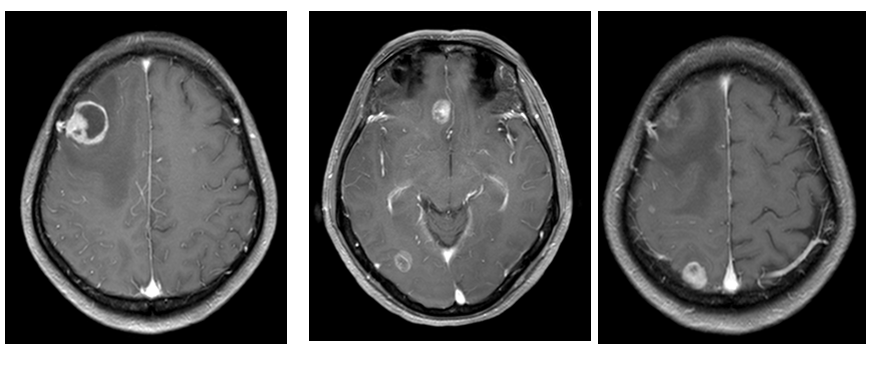
患者基线头颅MRI
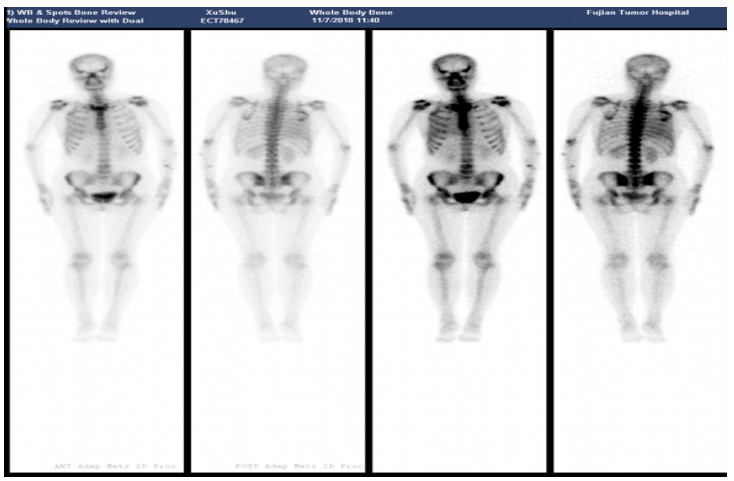
患者基线全身骨ECT
病理: (右上叶后段支气管活检)腺癌。IHC:K7+,NapsinA+,TTF-1+,P40-,P63,Ki67约60%+。
肺组织二代测序(NGS):EGFR 19del(50.5%)。
诊断:右肺腺癌伴右肺门、纵隔、双锁骨区淋巴结转移骨、肝、脑多发转移并右肺阻塞性肺炎及右侧胸腔积液cT2N3M1c IVB期(EGFR19del,ALK、ROS1野生型)。

该患者初诊时诊断为肺腺癌伴右肺门、纵隔、双锁骨区淋巴结转移骨、肝、脑多发转移并右肺阻塞性肺炎及右侧胸腔积液(cT2N3M1c IVB期),EGFR 19del突变。因此一线治疗为患者选择一代EGFR-TKI 埃克替尼靶向治疗并且配合全脑姑息放疗,疗效评估为PR,PFS为11个月。2019年11月,患者肺部原发灶稍进展,二线改用奥希替尼靶向治疗,血液基因检测未检出靶点。
2020年8月,患者肺部原发灶及肝转移灶稍进展,采用奥希替尼联合贝伐珠单抗治疗至2020年10月23日。2020年11月患者复查CT显示肿瘤进展,患者开始接受培美曲塞+卡铂+贝伐珠单抗三线治疗。三线治疗疗效不佳,1周期后快速进展。2020年12月18日,患者接受多西他赛四线治疗,最佳疗效为SD,PFS为3个月。2021年3月,患者复查MRI示,脑多发转移较前增多。2021年3月30日至2021年8月4日,患者接受安罗替尼联合替吉奥五线治疗4周期,期间配合脑转移灶调强放疗以及腰部转移灶调强放疗。
2021年9月,患者原发灶、肝转移灶、肾上腺转移灶进展,因此接受阿美替尼联合安罗替尼六线靶向治疗1周期,因肌酸激酶明显升高,停用阿美替尼。2021年10月,患者接受MET扩增基因检测,采用ddPCR对患者的血液进行检测,结果显示患者MET扩增(拷贝数2.6),七线治疗接受奥希替尼联合赛沃替尼治疗至今,疗效评估为SD。
病例提供专家
黄章洲教授:精准治疗时代,动态基因检测助力晚期肺癌患者全程管理
随着基因检测技术的迅速发展,非小细胞肺癌(NSCLC)的诊治已发生翻天覆地的变化,对于EGFR突变患者,EGFR-TKI是标准的一线治疗方式。本例患者初诊时为EGFR 19del突变,一线治疗采用一代EGFR-TKI药物埃克替尼治疗达到PR,PFS为11个月。但是这类患者在治疗过程中不可避免会发生获得性耐药,研究显示,MET扩增时EGFR-TKI治疗后的耐药机制之一,一/二代EGFR-TKI耐药后发生率为5%-21%[1-2],三代EGFR-TKI耐药后发生率为15%-30%[3-4]。同时抑制MET和EGFR或许是针对EGFR-TKI耐药后MET扩增患者的一种治疗策略。
本例患者经过多线治疗,自二线治疗后,更换多种治疗方案均快速进展,疗效不佳。之后患者进行血液ddPCR基因检测,结果显示为MET扩增。患者七线接受MET抑制剂赛沃替尼+奥希替尼治疗至今,患者疾病得到了良好的控制,肿瘤SD,PFS达到9个月,目前仍在治疗及积极随访中。可见,赛沃替尼+奥希替尼双靶治疗方案为这类超后线治疗的晚期肺癌患者带来了良好的治疗获益。
本例患者的治疗经过表明,驱动基因阳性的NSCLC患者治疗过程应该多次进行动态的基因检测,以更好地为患者选择针对性的治疗方案,达到精准治疗以及全程管理的目的,延长患者生存时间。
专家点评
庄武教授:超后线治疗的EGFR-TKI耐药伴MET扩增患者,赛沃替尼+奥希替尼有效控制病情,助力患者延长生存
既往报道显示,对于MET扩增引发的EGFR-TKI耐药人群,MET-TKI联合EGFR-TKI是有效的治疗策略。高选择性MET抑制剂赛沃替尼的获批上市打破了MET扩增患者“无药可用”的治疗困境,为这类患者带来了新的治疗选择。TATTON研究[5]探索了赛沃替尼+奥希替尼治疗EGFR-TKI耐药后MET扩增患者的疗效和安全性,结果显示,对于缺乏标准治疗方案的奥希替尼耐药后伴MET扩增人群,赛沃替尼+奥希替尼治疗仍可带来33%的客观缓解率(ORR)以及5.5个月的PFS,此外耐受性良好。这提示,即使针对多线治疗的患者,赛沃替尼联合奥希替尼仍能带来疗效和安全性获益。
本例患者初诊时为EGFR 19del突变,在经过一线、二线EGFR-TKI靶向治疗后,患者不可避免地面临EGFR-TKI耐药的困局,此时血液基因检测并未发现驱动基因,患者只能采用标准化疗、抗血管生成药物或放疗等方案,疗效不尽如人意,多线方案均失败。
患者经过多线治疗后,通过ddPCR检测方法检测出MET扩增,随后接受赛沃替尼联合奥希替尼治疗,病情得到了良好的控制,并且未出现明显的副作用,耐受性良好。至今患者仍在接受治疗并且积极随访。这再次验证了赛沃替尼联合奥希替尼双靶治疗的疗效和安全性。
同时也提醒临床医生,MET扩增是EGFR-TKI靶向治疗的常见耐药机制,临床上需要注重MET扩增的检测。虽然MET扩增检测目前首选FISH检测,但因组织标本不可及等原因,可考虑血液NGS、ddPCR等检测方法。
期待未来赛沃替尼这类高效低毒的靶向药物能够继续开展临床研究,为EGFR-TKI耐药患者带来更大的获益。
点评专家简介

庄武 教授
福建省肿瘤医院胸部肿瘤内科 行政主任、主任医师
中国老年学和老年医学学会精准医疗分会副主任委员
中国医师学会肿瘤多学科诊疗专业委员会常委
中华肺癌学院学术委员
TLCR肿瘤内科顾问委员会委员
福建省抗癌协会肺癌专业委员会常委
中国医疗保健国际交流促进会肺癌预防与控制分会委员
CSCO食管癌专业委员会委员
福建省海协会肿瘤临床诊疗分会副主任委员
北京肿瘤防治研究会常务委员
中国精准医学专业委员会常务委员
中国老年医学会康复分会食管癌康复专委会常务委员
福建省海协会肿瘤防治协会常务委员
福建省台海医学会常务委员
中国中药协会肿瘤药物研究专委会常务委员
国际肺癌研究协会(IASLC)会员
《肿瘤学杂志》常务编委
病例提供专家简介

黄章洲 教授
福建省肿瘤医院胸部肿瘤内科 副主任医师
福建省抗癌协会第二届肿瘤内科专业委员会委员
福建省抗癌协会肺癌专业委员会第二届、第三届青年委员会委员
中国老年学和老年医学学会精准医疗分会委员
中国中药协会肿瘤药物研究专业委员会委员
泛三角胸部肿瘤联盟专业委员会委员
泛长三角胸部肿瘤联盟专业委员会非小细胞肺癌罕见靶点学组委员
福建省首届小细胞肺癌中青年联盟成员
福建省海峡肿瘤防治科技交流协会精准医学专业委员会委员
福建省抗癌协会第一届康复委员会委员
福建省海峡医药卫生交流协会临床肿瘤学诊疗分会理事
参考文献:
[1].Pasquini G, Giaccone G. C-MET inhibitors for advanced non-small cell lung cancer[J]. Expert Opin Investig Drugs. 2018;27(4):363-375.
[2].Bean J, Brennan C, Shih JY, et al. MET amplification occurs with or without T790M mutations in EGFR mutant lung tumors with acquired resistance to gefitinib or erlotinib[J]. Proc Natl Acad Sci U S A. 2007;104(52):20932-7.
[3].Ramalingam SS, Cheng Y, Zhou C, et al. Mechanisms of acquired resistance to first-line osimertinib: preliminary data from the phase III FLAURA study. 2018 ESMO Congress. Abstract LBA50.
[4].Wang Y, Li L, Han R, et al. Clinical analysis by next-generation sequencing for NSCLC patients with MET amplification resistant to osimertinib[J]. Lung Cancer. 2018;118:105-110
[5].Lecia V Sequist, Ji-Youn Han, et al. Osimertinib plus savolitinib in patients with EGFR mutation-positive, MET-amplified, non-small-cell lung cancer after progression on EGFR tyrosine kinase inhibitors: interim results from a multicentre, open-label, phase 1b study[J]. Lancet Oncol. 2020;21(3):373-386.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |