*仅供医学专业人士阅读参考
MET扩增引发的奥希替尼耐药,该如何应对?
三代EGFR-TKI奥希替尼是国内外指南一致推荐的EGFR突变阳性晚期非小细胞肺癌(NSCLC)标准一线治疗方案,生存获益显著且安全性良好,自上市以来造福了无数患者。然而,由于其耐药机制较为复杂,部分医生担心耐药后“无药可用”,因此不愿“好药先行”。实际上,随着越来越多耐药后治疗策略的研发,针对不同的耐药机制,目前临床上往往已经有多种解决方案可选。本文聚焦奥希替尼一线治疗耐药后常见的MET扩增,介绍耐药应对策略,力求临床医生对耐药无忧。
从临床试验到真实世界,奥希替尼一线治疗获益明显
随着FLAURA研究结果公布,奥希替尼继获批用于二线治疗后,强势进军一线。数据显示,奥希替尼一线治疗EGFR突变阳性晚期NSCLC的中位无进展生存期(PFS)达18.9个月,较一代EGFR-TKI显著延长8.7个月,且所有亚组人群均显著获益[1]。此外,奥希替尼还是首个有总生存期(OS)显著获益的EGFR-TKI,中位OS达38.6个月(图1)[2]。
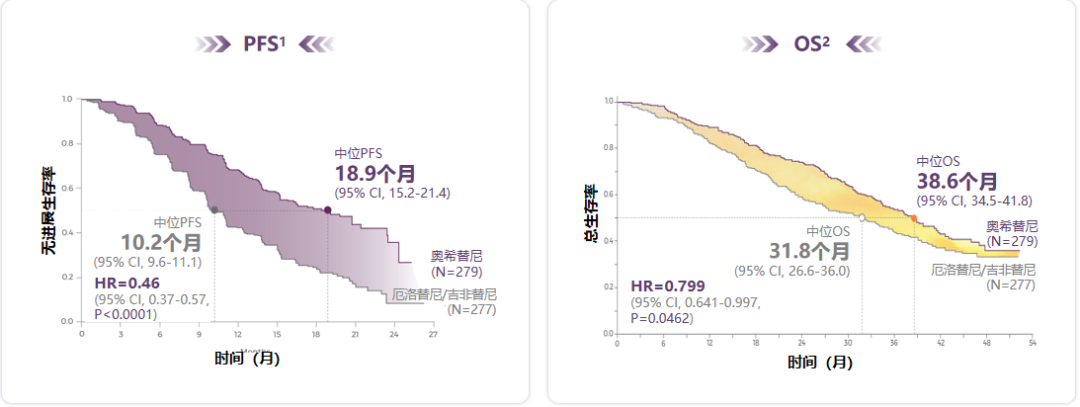
图1.奥希替尼PFS获益明确,并成功显著延长患者中位OS
不仅如此,奥希替尼一线治疗还具有显著的中枢神经系统(CNS)获益,可以显著降低52%的CNS进展或死亡风险,并且可能减少新发CNS病灶的出现[3,4]。与此同时,虽然与一代EGFR-TKI相比,奥希替尼暴露时间更长,但仍显示出良好的安全性,且患者生活质量改善[1,2,5]。据此,奥希替尼成为多部国内外权威指南一致高级别证据推荐的一线优选方案,引领EGFR突变晚期NSCLC一线治疗。
除此之外,奥希替尼在临床实践中也表现出同样优异的疗效和安全性。在近日召开的2022年欧洲肿瘤内科学会(ESMO)上,一项关于奥希替尼一线治疗中国人群的真实世界研究(FLOURISH研究)中期分析结果公布。研究结果显示,总人群的客观缓解率(ORR)为60.0%,疾病控制率(DCR)为96.3%。在中位随访10.2个月后,患者的1年PFS率为78.8%。在存在CNS转移的患者中,ORR和DCR分别为60.0%和95.0%,1年PFS率为78.9%;在无基线CNS转移的患者中,ORR和DCR分别为60.0%和97.5%,1年PFS率77.7%(图2)[6]。

图2. 总人群(左)和基线有/无CNS转移人群(右)的ORR、DCR和1年PFS率
无论是在总人群中,还是在存在CNS转移的人群中,奥希替尼一线治疗EGFR突变阳性晚期NSCLC均显示了与FLAURA研究相似的临床疗效,且没有新的安全信号。
奥希替尼耐药后,有多少患者会出现MET扩增?
虽然奥希替尼一线治疗的获益显著,但耐药似乎是绝大部分接受靶向治疗的患者难以逃脱的“宿命”。MET扩增被认为是奥希替尼治疗的重要耐药机制,不过目前尚缺少MET扩增与奥希替尼耐药的大样本的队列研究。
FLAURA研究显示,奥希替尼一线治疗获得性耐药后,MET扩增(15%)为最常见的耐药机制[7]。2020年发表的⼀篇⼩样本量分析发现,奥希替尼⼀线治疗获得性MET扩增的患者⽐例⾼达66%(组织-多区域全外显⼦组和RNA测序)[8]。一项综述总结了EGFR突变晚期NSCLC患者奥希替尼耐药的分子机制(组织和/或血浆检测),结果显示,奥希替尼一线治疗耐药后MET扩增的发生率为7%-15%(图3)[9]。
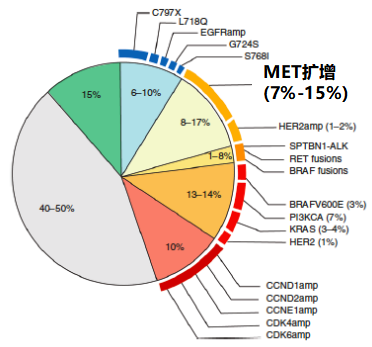
图3. 奥希替尼一线治疗耐药机制
Ⅱ期平台研究ORCHARD中采集患者在一线奥希替尼耐药后的肿瘤或血浆样本,通过二代测序(NGS)检测探索性分析了患者的耐药机制,其中组织检测结果发现,MET扩增的发生率为24%,是最普遍的耐药机制[10]。
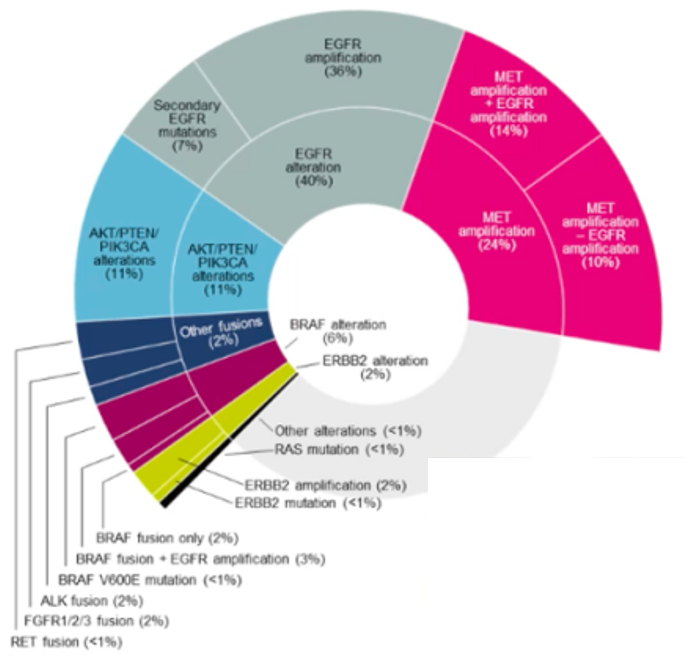
图4. ORCHARD研究中肿瘤组织NGS检测的奥希替尼一线耐药突变频率
另外,需要指出的是,MET扩增还可以发生在奥希替尼二线治疗耐药后,发生率为5%-50%[9]。MET扩增也是一/二EGFR-TKI获得性耐药分子机制中,除T790M外最重要的靶点之一,发生率为5%-20%[11,12]。因此,掌握EGFR-TKI耐药后MET扩增的应对策略至关重要。
克服MET扩增所致耐药,EGFR/MET双通路抑制展现实力
以往EGFR-TKI耐药后MET扩增的NSCLC患者以化疗为主,但获益有限。随着MET-TKI的研发,为此类患者的治疗带来了新思路。研究显示,EGFR和MET通路的双靶抑制可能带来协同治疗获益。
TATTON是一项多臂、多中心、开放标签、Ⅰb期研究,共纳入患者180例。该研究B1部分纳入三代EGFR-TKI治疗失败的患者(n=69),其中96%是二线及以上使用三代EGFR-TKI后进展的患者,且有52%的患者入组时已伴有脑转移。研究结果显示,对于三代EGFR-TKI耐药后MET扩增的NSCLC患者,奥希替尼联合赛沃替尼治疗的ORR为33%,中位PFS为5.5个月[13]。
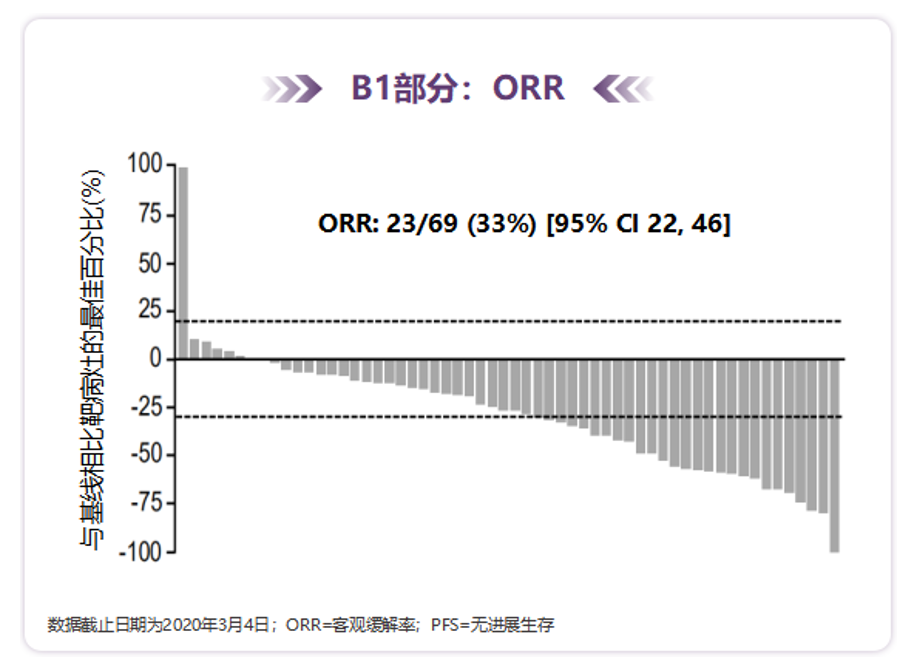
图5. TATTON研究最终分析结果
ORCHARD是一项开放标签、多中心、多药物、生物标志物指导的Ⅱ期临床试验,研究纳入经奥希替尼一线单药治疗后耐药的EGFR突变晚期NSCLC。结果显示,奥希替尼联合赛沃替尼用于奥希替尼一线治疗耐药且存在MET扩增患者的ORR可达41%(均确认部分缓解),目前所有确认部分缓解的患者仍在治疗中[14]。

图6. ORCHARD发现,奥希替尼+赛沃替尼在一线奥希替尼耐药患者中显示活性
SAVANNAH是一项探索赛沃替尼联合奥希替尼用于因MET扩增或过表达引起的奥希替尼治疗进展患者 (NCT03778229) 的单臂、开放标签、II 期临试验。在2022年世界肺癌大会(WCLC)上公布的SAVANAH研究初步结果显示,奥希替尼联合赛沃替尼双靶治疗在MET高扩增/高过表达(IHC 90+和/或FISH 10+)人群中展现出具有前景的临床疗效,ORR为49%,中位缓解持续时间(DoR)为9.3个月,中位PFS为7.1个月[15]。
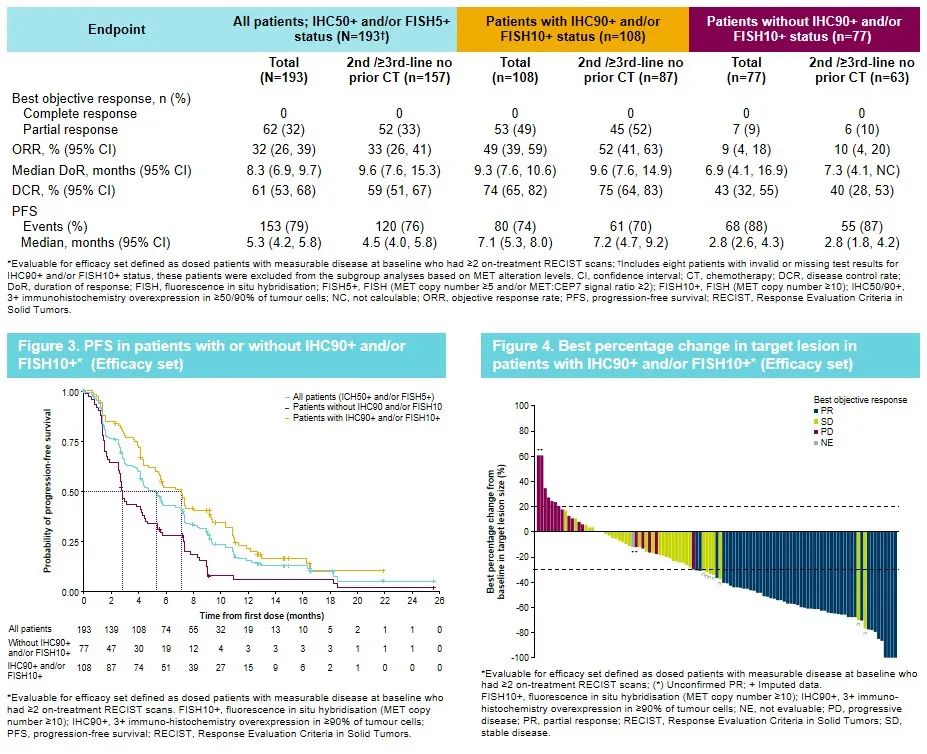
图7. SAVANNAH研究疗效数据
CHRYSALIS研究探索了Amivantamab联合Lazertinib治疗奥希替尼耐药后MET扩增的NSCLC的疗效与安全性,结果发现,45例患者接受Amivantamab联合Lazertinib治疗的ORR为36%,中位DoR为9.6个月,临床获益率(CBR)为64%,中位PFS为4.9个月,且安全性可控[16]。
此外,INSIGHT 2是一项双臂、开放标签、II 期临试验,旨在评估Tepotinib联合奥希替尼治疗奥希替尼获得性耐药合并MET扩增的晚期或转移性NSCLC患者的疗效。该研究结果在近日召开的2022年ESMO大会上以LBA的形式公布,Tepotinib联合奥希替尼展现出较高的抗肿瘤活性且耐受性良好[17]。
专家点评:EGFR/MET双通路抑制有望突破耐药壁垒,使一线奥希替尼耐药后MET扩增治疗无忧
MET扩增是EGFR-TKI耐药的重要机制之一,如何克服耐药已成为当下的学术热点。EGFR联合MET双通路抑制有望突破耐药壁垒,逆转耐药进程,恢复肿瘤缓解,进一步提升EGFR-TKI耐药后MET扩增患者的生存获益。目前已经有多项研究证实,MET-TKI联合EGFR-TKI(如奥希替尼联合赛沃替尼)具有良好的抗肿瘤活性。美国国家综合癌症网络(NCCN)指南中也对EGFR-TKI耐药后MET扩增患者建议MET-TKI联合EGFR-TKI治疗[18]。而且,更多的联合治疗方案正在探索中,有望给临床治疗带来更多选择。
由此可见,目前对于奥希替尼耐药后MET扩增的NSCLC已经不再“无药可用”,因此临床医生对于一线使用奥希替尼无需太多顾虑。奥希替尼一线治疗的临床获益已经在FLAURA研究和真实世界研究中得到证实,临床实践中将“好药先行”可能给EGFR突变阳性的患者带来更大获益。
专家简介

林英城 教授
副院长,内科主任
主任医师,硕士导师
汕头大学医学院附属肿瘤医院
广东省医学会肿瘤分会副主任委员
广东省临床医学会精准医疗专委会副主任委员
广东省胸部肿瘤防治研究会副会长
广东抗癌协会癌症康复和姑息治疗专委会副主任委员
广东省健康管理学会肿瘤防治专业委员会副主任委员
广东省药学会乳腺癌临床用药指导委员会副主任委员
广东省抗癌协会化疗专业委员会名誉副主任委员
广东省精准医疗应用学会结直肠专委会常务委员
中国南方肿瘤合作组(CSWOG) 常务委员
中国临床肿瘤学会( CSCO )委员
中国抗癌协会化疗专业委员会委员
中国抗癌协会癌症康复和姑息治疗专委会委员
中国医师协会外科MDT专委会委员
参考文献:
[1].Soria et al. N Engl J Med 2018;378:113-25
[2].Suresh S Ramalingam, et al,. N Engl J Med. 2020 Jan 2;382(1):41-50
[3].Reungwetwattana T, et al. J Clin Oncol 2018 Aug 28;JCO2018783118.
[4].2. J Vansteenkiste at ESMO Asia 2017
[5].Natasha B Leighl, et al,. Eur J Cancer. 2020 Jan;125:49-57.
[6].Jianying Zhou, et al. 2022ESMO.1123P.
[7].Ramalingam SS, et al. 2018 ESMO. LBA50.
[8].Roper N, et al. Cell Rep Med. 2020 Apr 21;1(1):100007
[9].Leonetti A, et al. Br J Cancer. 2019 Oct;121(9):725-737.
[10].R. J. Hartmaier, et al, 2022 AACR, Poster# LB078/3
[11].Westover D, et al. Ann Oncol. 2018 Jan 1;29(suppl_1):i10-i19.
[12].Matikas A, et al. Clin Lung Cancer. 2015 Jul;16(4):252-61.
[13].Lecia V Sequist, et al. Lancet Oncol. 2020;21(3):373-386.
[14].Helena A Y, et al. ESMO 2021, Abstract 1239P.
[15].Ann M J, et al. WCLC 2022. EP08.02-140.
[16].Bauml J, et al. 2021 ASCO. Abstract 9006.
[17].Tepotinib + osimertinib for EGFRm NSCLC with MET amplification(METamp) after progression on first-line(1L)osimertinib:Initial results from the INSIGHT 2 study. 2022 ESMO,LBA52.
[18].NCCN Clinical Practice Guidelines in Oncology: Non-Small Cell Lung Cancer. Version 4. 2022.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |