*仅供医学专业人士阅读参考
优YOUNG好医声——晚期结直肠癌全程管理病例演讲巴蜀云浙站强势来袭,多位专家共话晚期CRC诊疗新策略,充分交流诊疗新理念。
为践行国家大健康战略之肿瘤慢病化管理,规范和提高晚期结直肠癌(CRC)全程管理水平,探索新型诊疗思路,展现青年医生临床诊疗思维以及演讲风采。由中国临床肿瘤学会结直肠癌专委会与和黄医药携手举办的“优YOUNG好医声——晚期结直肠癌全程管理病例演讲”项目在今年持续优化,重磅来临。8月28日,晚期结直肠癌全程管理病例演讲“巴蜀云浙站”线上火热开启,浙江大学医学院附属邵逸夫医院潘宏铭教授和四川大学华西医院邱萌教授携手担任大会主席。

图1 浙江大学医学院附属邵逸夫医院潘宏铭教授 开场致辞

图2 四川大学华西医院邱萌教授 开场致辞
晚期结直肠癌全程管理病例演讲——激烈交锋,引人入胜
竞技比拼病例演讲环节在重庆市中医院辇伟奇教授的主持下正式开启。由昆明医科大学第二附属医院梁道明教授、重庆医科大学附属第二医院王亚旭教授、四川省人民医院谢可教授、丽水市中心医院谢艳茹教授、湖州市第一人民医院徐永强教授和浙江大学医学院附属杭州市第一人民医院郑松教授组成评审团,针对各位演讲嘉宾的表现进行点评并给出评分。
病例一:一例晚期直肠癌的病例分享
该病例由四川省自贡市第四人民医院提供。
导师:缪继东教授,演讲:周晓波医生。
该患者为直肠腺癌,2014年6月于外院行直肠癌根治术,术后行辅助化疗4疗程。2017年至2018年期间,患者因直肠癌肝转移于外院行肝肿瘤射频消融术3次并且口服阿帕替尼靶向治疗,基因检测结果显示为KRAS突变、微卫星稳定(MSS)、VEGFR(+)。
2021年,患者疾病进展,入院后诊断为直肠腺癌伴肝转移及胸膜转移rIV期,接受卡培他滨+贝伐珠单抗+营养支持姑息治疗后1个月双侧胸膜病灶进展;随后给予患者一线XELOX+贝伐珠单抗2疗程后复查提示:双肺多发结节,考虑出现转移;一线治疗进展后,二线给予患者mXELIRI+贝伐珠单抗治疗3疗程治疗,复查提示患者肿瘤病灶再度发生进展;三线治疗的选择成为患者延长生存时间,改善生存质量的关键,诊疗组为患者选择呋喹替尼单药治疗。2个月后患者影像学复查疗效评估达到部分缓解(PR),且至今药物带来的生存获益仍在继续。该真实世界诊疗病例提示:三线呋喹替尼治疗能够为多发转移CRC患者带来极佳的肿瘤控制效果。

图3 四川省自贡市第四人民医院周晓波医生做病例演讲
病例二:“爱”回路转,“呋”摇直上
该病例由浙江大学医学院附属第二医院提供。
导师:陈佳琦教授,演讲:张彦医生。
该病例是乙状结肠癌伴髂血管旁、腹膜后淋巴结、右下肺转移患者,cT3N2bM1b期,行腔镜下原发灶切除术,基因检测结果为:KRAS G13D突变、Her-2阴性、MSS,术后分期为pT3N2M1b。
一线为患者选择:贝伐珠单抗+FOLFIRI联合治疗方案4周期,疗效评估达到PR,治疗过程中患者出现IV度粒缺性发热及腹泻。同时,完善基因检测结果为UGT1A16,28位点杂合突变。因此,进行伊立替康减量和预防性长效升白治疗。一线治疗12个周期后,考虑到患者伊立替康不耐受且瘤负荷较小,结合患者意愿暂停全身治疗,建议定期随访,半年后复查患者左下肺新发结节,4个月后结节增大,考虑肠癌肺转移,行SBRT治疗后结节缩小。停药20个月后,患者疾病全面进展,二线治疗行贝伐珠单抗+XELOX方案6周期后,疗效评为疾病进展(PD)。三线治疗为患者选择呋喹替尼+信迪利单抗联合策略,3.5个月后疗效评估显示仍为PD。于是在四线在原有呋喹替尼+信迪利单抗联合方案基础上加入卡培他滨。截至目前患者已接受16个周期联合治疗,疗效评估达到PR,无进展生存时间(PFS)达到14个月,且该患者总OS已达到54个月。提示后线抗血管生成联合免疫及化疗,有望成为反复进展的难治mCRC患者药物治疗优选方案。

图4 浙江大学医学院附属第二医院张彦医生做病例演讲
病例三:道阻且“肠”,行则将至
该病例由云南省肿瘤医院提供。
导师:胡凤娣教授,演讲:李蓉医生。
该病例是右半结肠腺癌伴肝肺以及淋巴结多发转移的患者,CT3N+M1b IVB期,基因检测结果提示:KRAS、NRAS、BRAF均为野生型。
患者完善检查后,一线给予西妥昔单抗+mFOLFOX6方案治疗8周期,疗效评估显示达到PR,经过院内MDT讨论暂不考虑手术以及放疗。一线治疗12周期后,行卡培他滨+西妥昔单抗维持治疗,在维持治疗2周期后复查影像学显示进展,疗效评估:PD。
进入二线治疗后,患者接受贝伐珠单抗+FOLFIRI 方案8周期治疗,随访复查仍提示疾病进展,疗效评估:PD,后续换用西妥昔单抗+FOLFIRI方案治疗后,肿瘤仍旧快速进展。
三线治疗,为患者选择呋喹替尼+信迪利单抗联合治疗,疗效评估为SD,肿瘤控制情况良好。遗憾的是,患者在4个周期后疾病再度进展,肝肺转移增多增大。由于患者肿瘤负荷主要集中于肝脏和肺部,充分沟通后行7周期肝动脉HAIC治疗以及2次肺部碘125粒子植入术,治疗期间疾病得到控制。目前该患者采用瑞戈非尼全身治疗控制病情,总OS已超过24个月。在给予患者呋喹替尼联合免疫治疗期间,患者获得较好的肿瘤控制效果。提示呋喹替尼+免疫或为上述患者提供全新的治疗思路。
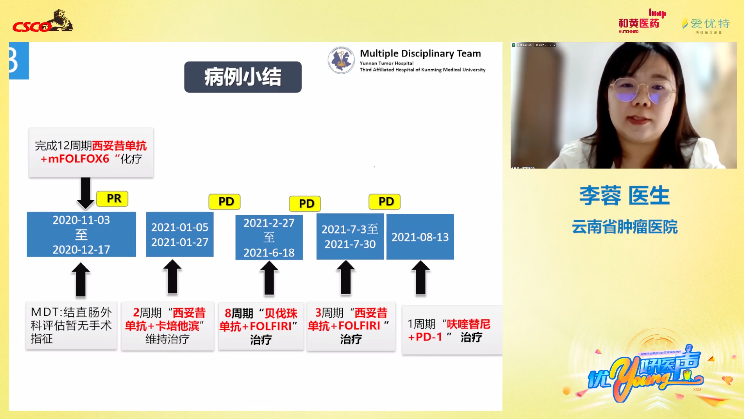
图5 云南省肿瘤医院李蓉医生做病例演讲
病例四:我和他以及它的故事——记一例晚期直肠癌多线治疗的实践与思考
该病例由浙江大学医学院附属第一医院提供。
导师:蒋海萍教授,演讲:李宁医生。
该病例为直肠腺癌伴肝脏多发转移的患者,cT3N0M1 IV期,基因检测结果为KRAS、NRAS、BRAF野生型。一线治疗方案给予患者西妥昔单抗+mFOLFOX6方案治疗,疗效评估为PR,后行西妥昔单抗单药维持治疗。
一线治疗为患者带来了13.7个月的PFS。维持治疗6个月后复查提示肿瘤进展,二线采用伊立替康+雷替曲塞+贝伐珠单抗治疗,仅3.5个月后,患者复查提示肿瘤再度进展,疗效评估为PD。
二线治疗失败后,给予患者呋喹替尼+卡瑞利珠单抗三线治疗,治疗期间肝脏病灶显著缩小,疗效评估为PR,PFS达到21个月之久。四线给予患者TAS-102+贝伐珠单抗治疗,仅仅带来2个月的PFS获益。
五线患者入组IBI321研究,接受CD137单抗靶向治疗。截止目前疗效评估为SD,PFS 5.3个月。从该临床诊疗案例不难看出,在一、二线均治疗失败后,呋喹替尼为患者带来了治疗进程中最长的一段PFS时间。体现了呋喹替尼良好的肿瘤控制效果与极佳的药物安全性。
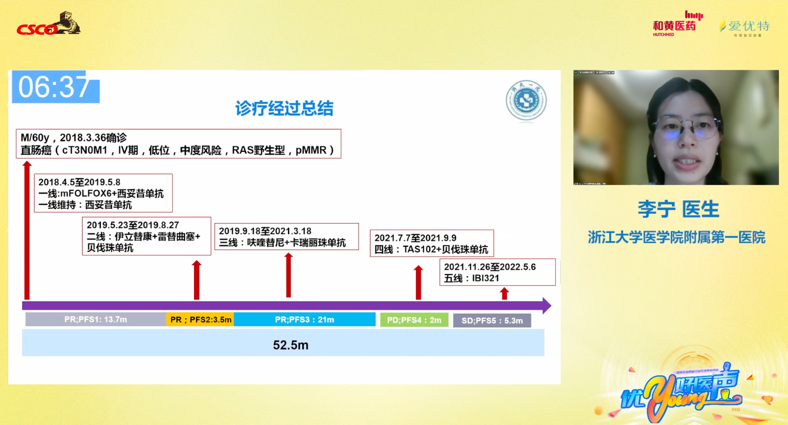
图6 浙江大学医学院附属第一医院李宁医生做病例演讲
病例五:山穷水尽疑无路,柳暗花明又一村——晚期肠癌全程管理病例分享
该病例由浙江省台州市第一人民医院提供。
导师:唐小万教授,演讲:章展医生。
该病例为直肠癌伴肝脏转移患者,cT3NxM1b IVB期,基因检测结果为MSS、KRAS G12C突变。经过第一次MDT讨论,一线治疗给予患者mFOLFOX6+贝伐珠单抗方案治疗5周期,复查疗效评估为PR。但使用奥沙利铂期间,患者出现过敏性休克,因此更改化疗方案为mFOLFIRI方案,在随后的治疗期间患者肿瘤病灶显著缩小。期间于2020年12月5日为患者行肝脏转移瘤手术切除以及射频消融局部治疗。2021年2月再给予直肠癌根治术,术后病理提示直肠癌。术后继续予以mFOLFIRI治疗,围手术+术后辅助治疗共12周期。2021年8月,患者出现肺部多发结节。进入三线治疗后,为患者选择呋喹替尼单药治疗,截至目前已经为患者带来长达11个月的PFS时间,同时患者复查提示肿瘤控制良好,至今患者仍处于三线治疗获益中。上述真实世界诊疗病例提示,在晚期CRC患者中,三线呋喹替尼药物治疗为患者带来了显著的肿瘤控制效果,生存获益明显。
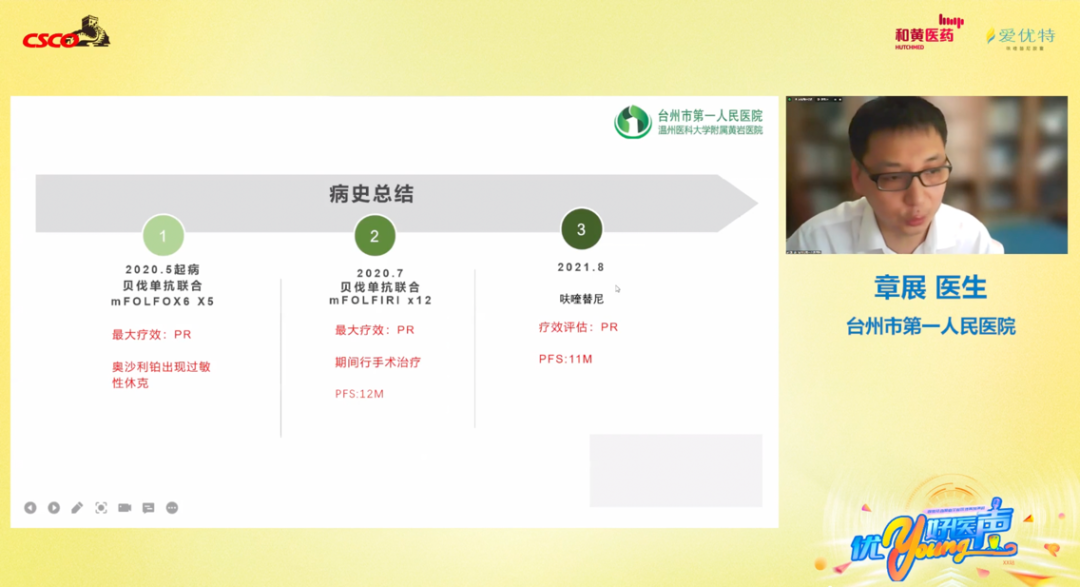
图7 浙江省台州市第一人民医院章展医生做病例演讲
病例六:“化疗假期”拨云见日——一例晚期直肠癌肝转移患者的治疗之路
该病例由陆军特色医学中心大坪医院提供。
导师:钱程远教授,演讲:苏晓娜医生。
该病例为低位直肠腺癌伴肝脏多发转移患者,cT3dN1M1 IV期,MDT讨论意见为转化治疗后评估有无手术指征。一线给予患者mFOLFOX6化疗2周期, 期间完善基因检测结果为MSS,KRAS、BRAF、NRAS野生型。第3周期患者行西妥昔单抗联合mFOLFOX减量方案治疗,后因患者肿瘤病灶无显著变化且不良反应无法耐受停药。二线给予西妥昔单抗+FOLFIRI(减量20%)方案治疗,2个月后患者肝转移灶增大增多。结合第二次MDT讨论结果,且考虑到患者耐受性,三线给予患者呋喹替尼联合替雷利珠单抗治疗,期间联合TACE治疗,后肝脏病灶稳定,直肠病灶略有增大,PFS迄今已达到20个月之久。该病例提示,晚期CRC患者后线接受呋喹替尼联合免疫治疗带来了长时间的肿瘤控制,且耐受性良好。
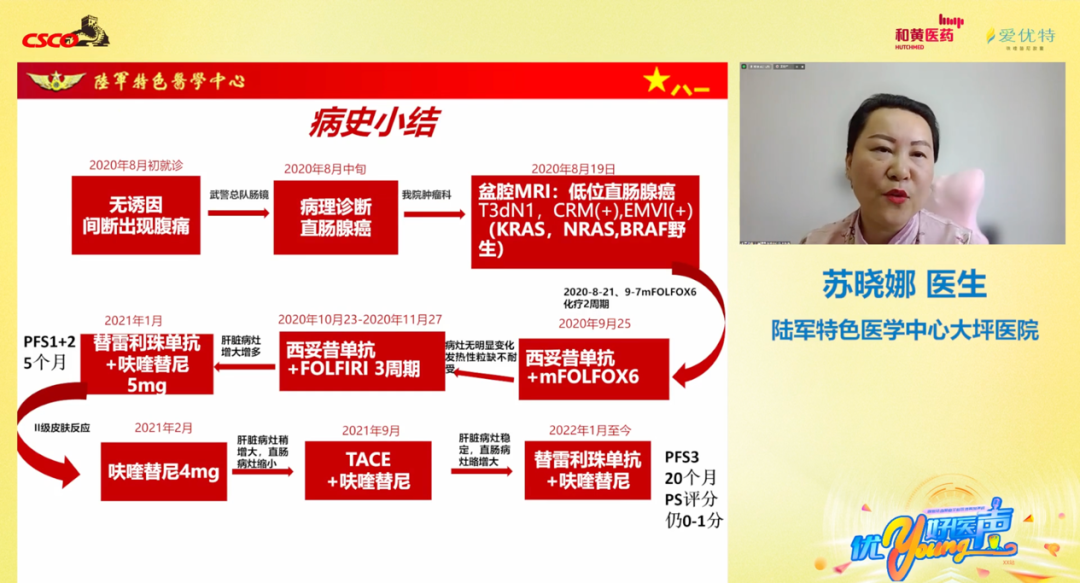
图8 陆军特色医学中心大坪医院苏晓娜医生做病例演讲
六组演讲嘉宾进行了精彩的结直肠癌诊疗病例分享,并且充分展示了诊疗团队在其中的全面思考和谨慎抉择。在后续提问和点评环节,演讲嘉宾之间互相切磋,你惑我解,精彩纷呈。演讲嘉宾与评审团充分互动,评审团提问与点评深入浅出,提纲挈领。最终经过评审团合议,来自浙江大学医学院附属第二医院的张彦医生最终拔得头筹,顺利进入全国总决赛。
图9 大会总结
随着会议进入尾声,大会主席潘宏铭教授和邱萌教授代表与会专家向张彦医生及其导师陈佳琦教授表示祝贺,并且对张彦医生在后续的演讲分享中的表现表示期待。同时,两位主席总结道,本次会议内容丰富详实,不乏对晚期CRC患者的人文关怀,希望各位医生在后续的病例展示中进一步加强规范化的诊疗和循证医学证据的积累。期待通过本次病例展示与交流,能够进一步推动晚期CRC全程管理的规范化,促进领域的发展,帮助更多CRC患者获益。
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |