*仅供医学专业人士阅读参考
免疫联合抗血管生成药物“组合拳”打破传统治疗格局。
一年一度的全球肿瘤界盛会--欧洲肿瘤内科学会(ESMO)大会9月在法国巴黎举行。上海交通大学医学院附属胸科医院韩宝惠教授牵头的一项SUNRISE研究入选ESMO大会口头报道,该研究为信迪利单抗联合安罗替尼对比含铂化疗一线治疗转移性非小细胞肺癌(NSCLC)的随机、对照研究[1],“医学界”诚邀韩宝惠教授分享对于该研究的相关见解。
免疫+抗血管强强结合,
Ⅰ期研究展现其令人鼓舞的疗效
近年来肺癌领域治疗进展迅速,免疫治疗、抗血管生成治疗等治疗手段层出不穷。肿瘤的生长和转移依赖于肿瘤新生血管的形成,抗血管生成治疗逐渐引起人们关注,但接受抗血管生成单药治疗的患者并未得到明显预后改善[2]。随着PD-1单抗、PD-L1单抗等相关药物获批,免疫检查点抑制剂已成为肺癌领域的研究热点,很大程度地改善了部分肺癌患者的预后,但免疫单药的治疗模式仅适用于PD-L1高表达人群,如何扩大免疫治疗响应人群是目前亟待解决的问题[3]。
抗血管生成药物联合免疫治疗在理论上可提高免疫治疗的疗效[4],临床前研究已证实免疫治疗与抗血管生成药物联合使用,具备协同增效作用,可发挥1+1>2的强强联合效果[5]。韩宝惠教授指出,在既往开展的I期研究[6]中,信迪利单抗联合安罗替尼在一线治疗驱动基因阴性的晚期NSCLC中展现出了令人鼓舞的疗效。该研究纳入22例未接受过治疗且没有EGFR/ALK/ROS1突变的IIIB/C或IV期NSCLC患者,接受信迪利单抗联合安罗替尼治疗,客观缓解率(ORR)为72.7%,疾病控制率(DCR)为100%,中位无进展生存期(PFS)为15个月。研究还观察到无论PD-L1表达如何,肿瘤突变负荷(TMB)高低,所有患者均能从联合治疗中获益且耐受性良好。
SUNRISE研究初步结果可圈可点,
疗效持久,安全可耐受
在该Ⅰ期研究成果的鼓舞下,为了进一步探索信迪利单抗联合安罗替尼一线治疗转移性NSCLC的疗效和安全性,达到临床治疗中“去化疗”的目的,韩宝惠教授团队开展了信迪利单抗联合安罗替尼对比标准化疗的SUNRISE研究[1]。韩宝惠教授表示,SUNRISE是一项开放标签、多中心、随机的Ⅱ期研究,纳入IV期、未经治疗的、EGFR/ALK/ROS1阴性的NSCLC患者。在入组患者方面,同时纳入了鳞癌和非鳞癌患者,还纳入了脑转移患者和肝转移患者,中位年龄在64-65岁。入组患者按照1:1随机分配至信迪利单抗联合安罗替尼组或含铂化疗组。化疗组的患者允许在疾病进展后交叉至信迪利单抗治疗,为患者争取到后线免疫治疗机会[1]。
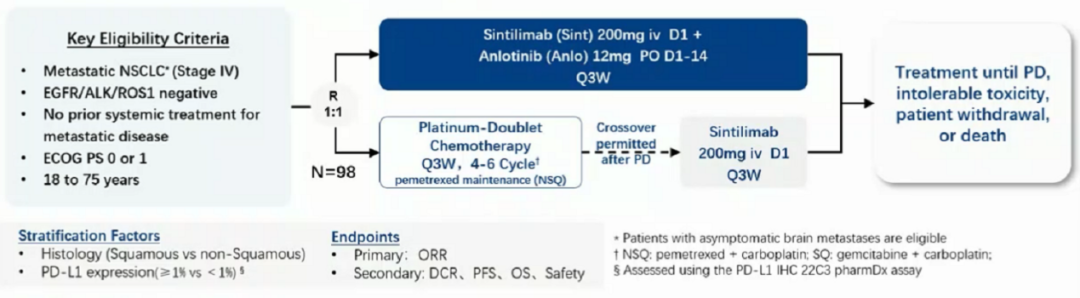
图1.SUNRISE研究设计
截至2022年7月15日,信迪利单抗联合安罗替尼组40例患者、化疗组43例患者可评估疗效。信迪利单抗联合安罗替尼组的ORR达到50%,化疗组的ORR为32.6%。且无论PD-L1表达情况如何,信迪利单抗联合安罗替尼组皆有获益。
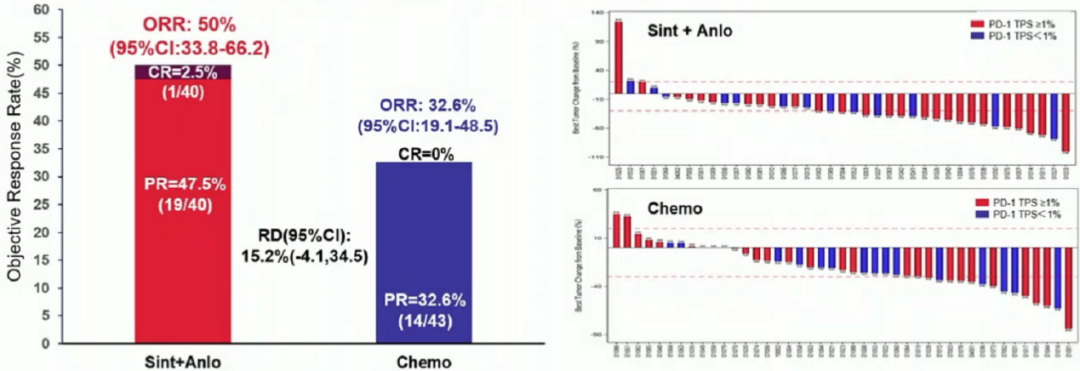
图2.信迪利单抗联合安罗替尼组和含铂化疗组的肿瘤缓解情况
信迪利单抗联合安罗替尼组和化疗组的中位缓解持续时间(DOR)分别为16.3个月和6.2个月,中位PFS分别为10.8个月和5.7个月,风险比(HR)为0.4,表明疾病进展风险下降60%,P=0.002[1]。

图3.信迪利单抗联合安罗替尼组和含铂化疗组的中位DOR和中位PFS
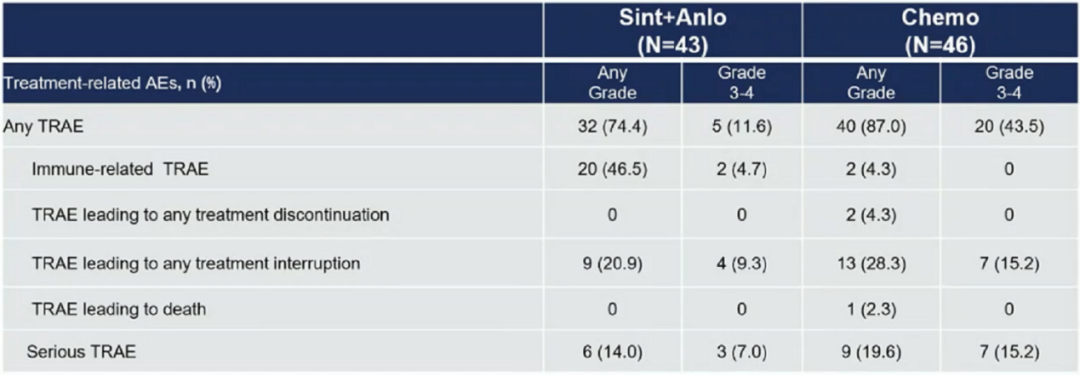
在安全性方面,信迪利单抗联合安罗替尼组和化疗组的治疗相关不良反应(TRAE)发生率分别为74.4%和87%,两组3-4级TRAE发生率分别为11.6%和43.5%。化疗组有2例患者因TRAE而停药,1例因TRAE死亡。信迪利单抗联合安罗替尼组并未发生相关事件,整体安全可耐受[1]。
表1.安全性总结
韩宝惠教授认为SUNRISE研究给我们带来了新思路——“去化疗”模式。相比传统化疗,免疫治疗具有应答持久、治愈率高、毒副反应小、患者生活质量高等多种优势,但免疫单药治疗疗效有限,且并非所有NSCLC患者都能从免疫治疗中受益,其受众仅为30%左右[7],被指南优先推荐用于PD-L1≥50%晚期NSCLC患者的一线治疗[8]。虽然免疫+化疗的治疗获益不受到PD-L1表达影响,但是化疗所带来的不良反应较大,医生和患者都希望有“chemo-free”方案可供选择。SUNRISE研究提示无论PD-L1表达情况如何,年龄偏大、体力评分较差的、不能耐受化疗或对化疗有顾虑的患者,若驱动基因为阴性可以考虑接受PD-1单抗联合抗血管生成药物治疗。相比化疗,信迪利单抗联合安罗替尼一线治疗NSCLC的疗效更高、中位PFS更长、安全性较好。期待SUNRISE研究的最终结果能够为目前的临床实践用药带来更多的指导意义,为晚期NSCLC患者治疗做出更多的贡献。
免疫治疗精准化任重而道远,
“去化疗”模式仍需继续探索
免疫联合抗血管生成治疗的“去化疗”模式是未来重要的诊疗策略之一,研究证实了抗血管生成治疗和免疫微环境息息相关,但并非每种免疫联合抗血管生成治疗方案都能让患者获益。韩宝惠教授举例了另一种免疫联合抗血管生成治疗方案的III期LEAP-007研究[9],该研究旨在探索PD-L1阳性(TPS≥1%)晚期NSCLC患者一线接受免疫联合抗血管生成治疗对比免疫联合安慰剂治疗的临床结局,总生存期(OS)为阴性结果。免疫联合抗血管生成药物的治疗模式不仅仅是两个药物的简单叠加,更需要关注的是药物间的独特组合是否能带来更佳的治疗效果,联合模式下疗效与毒副反应间如何达到平衡,这些都值得去反思的。
另外,肿瘤血管生成、机体免疫反应等与肿瘤内环境改变之间的关系复杂,还需要更系统的评估方法以精确定位获益人群。如何通过可靠的生物标记物来选择联合治疗方案的优势人群,如何选择抗血管生成药物和免疫治疗药物种类,确定用药的周期、顺序,药物剂量如何调整,同时联合用药安全性等问题都需要在未来不断探索和解决。
专家简介

韩宝惠 教授
上海市胸科医院
教授、博士生导师、呼吸内科名誉主任
上海市领军人才、优秀学科带头人
中华肺癌学院执行院长
CSCO肿瘤血管靶向专委会前任主委
中国抗癌协会肿瘤精准诊疗专委会副主委
亚太医学生物免疫学会肿瘤分会主委
上海市抗癌协会副理事长(第八届)
上海市医学会肿瘤靶分子专委会副主委,后任主委
上海市医师学会呼吸学会副会长
擅长肺癌诊断及多学科治疗,肺癌生物免疫靶向治疗及抗肿瘤新药临床研究。2014年获中华医学科技二等奖,第八届中国呼吸医师奖获得者;多次获上海市医学科技奖二三等奖。发表肺癌领域文章300余篇,牵头中华医学会《肺癌诊疗指南》主编《肿瘤生物免疫靶向治疗》《超声支气管镜技术》专著、主译《抗肿瘤新生血管治疗》,参编专著10余部
参考文献:
[1]Baohui Han,Tianqing Chu,Zhuang Yu,et al.Sintilimab plus anlotinib versus platinum-based chemotherapy as first-line therapy in metastatic NSCLC(SUNRISE):an open label,multi-center,randomized,phase 2 study.2022ESMO.
[2]王婧怡,彭文颖,江美林,邬麟.抗血管生成药物联合免疫检查点抑制剂治疗晚期非小细胞肺癌的研究进展[J].中国肺癌杂志,2021,24(3):196-203.
[3]Remon J,Passiglia F,Ahn MJ,et al.Immune Checkpoint Inhibitors in Thoracic Malignancies:Review of the Existing Evidence by an IASLC Expert Panel and Recommendations.J Thorac Oncol.2020;15(6):914-947.
[4]彭敏华,陈公琰.抗血管生成疗法与免疫疗法联合治疗晚期非小细胞肺癌的作用机制及应用研究进展[J].山东医药,2022,62(17):85-88.
[5]Manegold C,Dingemans A M C,Gray J E,et al.The potential of combined immunotherapy and antiangiogenesis for the synergistic treatment of advanced NSCLC[J].Journal of Thoracic Oncology,2017,12(2):194-207.
[6]Chu T,Zhong R,Zhong H,et al.Phase 1b Study of Sintilimab Plus Anlotinib as First-line Therapy in Patients With Advanced NSCLC.J Thorac Oncol.2021;16(4):643-652.
[7]赵沙,蒋涛,周彩存.抗PD-1/PD-L1免疫治疗疗效预测标志物在非小细胞肺癌中的研究进展[J].肿瘤,2016,7:823-828.
[8]NCCN Clinical Practice Guidelines in Oncology:Non-Small Cell Lung Cancer(Version 4.2022)
[9]T.Csoszi,J.C.Yang,A.Luft,et al.Pembrolizumab(Pembro)With or Without Lenvatinib(Lenva)in First-Line Metastatic NSCLC With PD-L1 TPS≥1%(LEAP-007):A Phase 3,Randomized,Double-Blind Study.2021 ESMO Abstract 120O.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |