*仅供医学专业人士阅读参考
医生有义务告知患者5年生存率。
2018年是晚期非小细胞肺癌(NSCLC)免疫一线治疗的“元年”,四个公认具有里程碑意义的III期临床研究:KEYNOTE-189、KEYNOTE-407、KEYNOTE-042、以及CheckMate-227相继公布研究结果。其中,KEYNOTE-189和KEYNOTE-407作为达到了主要研究终点的免疫检查点抑制剂联合含铂化疗一线治疗晚期NSCLC的全球多中心,随机双盲对照的III期临床研究,意义非凡。
在这四年间,免疫治疗改写了包括中国和美国在内的晚期鳞和非鳞NSCLC的治疗指南,使得免疫+化疗成为晚期NSCLC患者的标准一线治疗。
KEYNOTE-189和KEYNOTE-407的5年OS数据在2022年欧洲肿瘤内科学会(ESMO)年会公布[1,2],结果显示,帕博利珠单抗(K药)联合含铂化疗方案较含铂化疗可以带来更优的长期生存率,一线治疗晚期非鳞NSCLC或鳞状NSCLC的5年OS率分别为19.4% 和18.4%, 而化疗分别为11.3%和9.7%。
K药联合化疗方案成为全球首个具有5年OS率数据支持的免疫联合化疗一线治疗晚期NSCLC的方案。
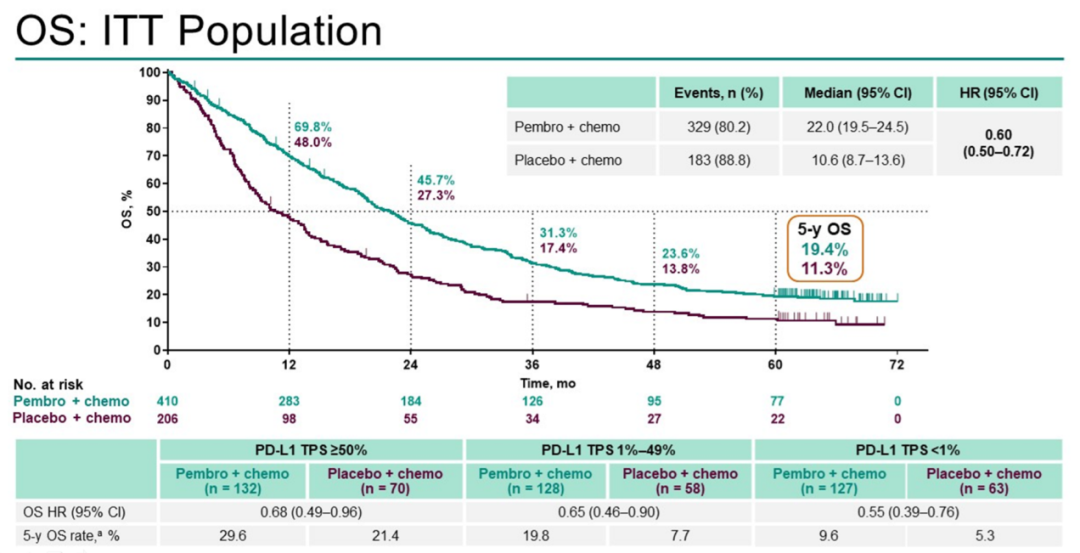
图1 KEYNOTE-189 5年OS1
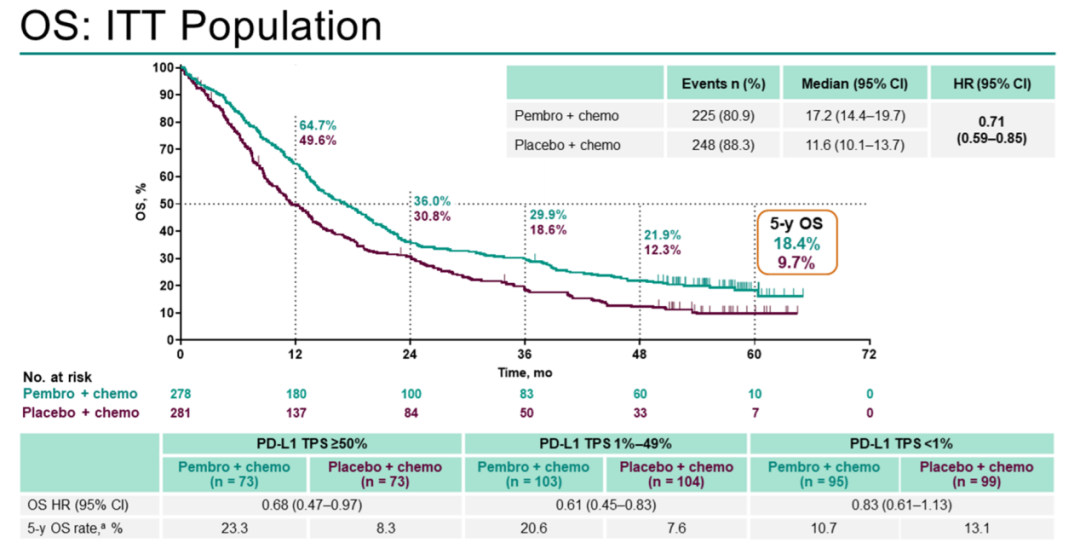
图2 KEYNOTE-407 5年OS2
同时公布的是KEYNOTE-189和KEYNOTE-407研究的5年PFS(无疾病进展生存)数据。 在第5年时,仍分别有7.5%和10.8%的非鳞和鳞状NSCLC患者没有出现疾病进展,而对照化疗组的5年PFS率分别为0.6%和3.5%。
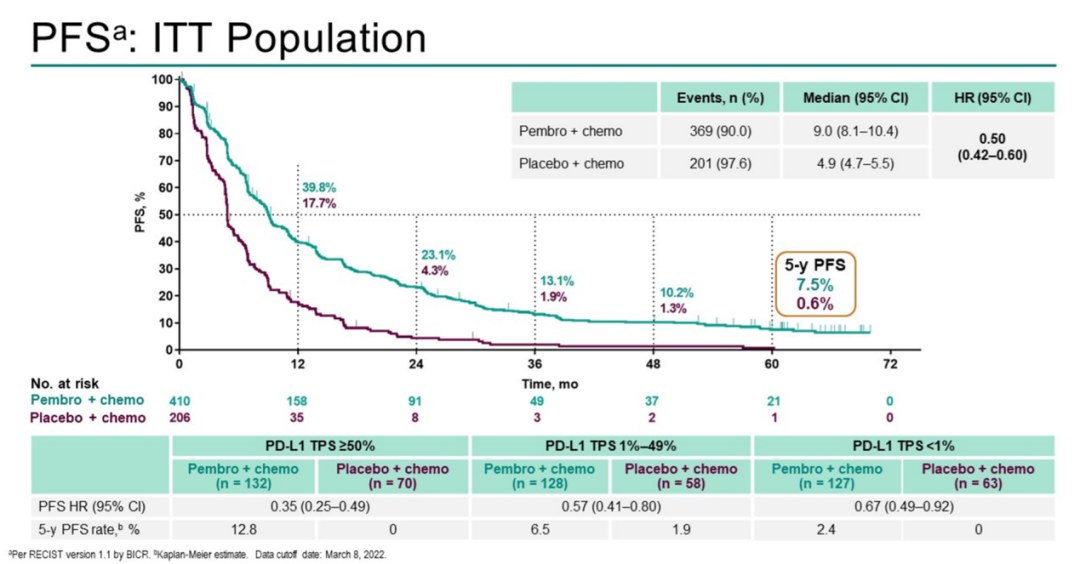
图3 KEYNOTE-189 5年PFS1
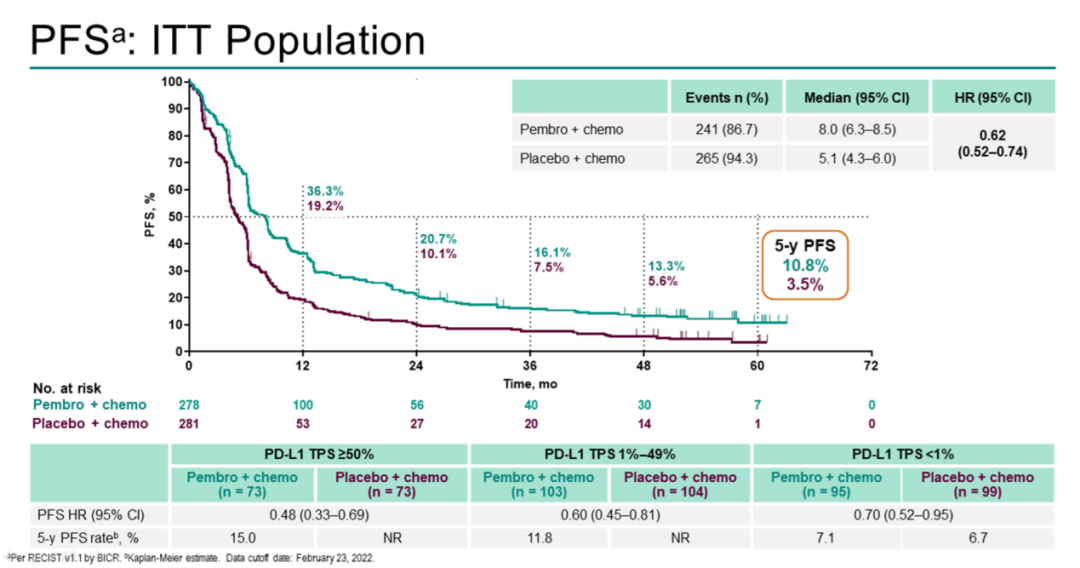
图4 KEYNOTE-407 5年PFS2
当前国内已有4个原研的PD-1单抗获批联合化疗一线治疗局部晚期或转移性NSCLC。 这些PD-1单抗的III期临床研究,无论是针对鳞状或非鳞NSCLC,其主要研究终点PFS, 而非OS, 并纳入了不同比例的IIIB和IIIC期患者[3-8]。
而目前仅有卡瑞利珠单抗联合卡铂和紫杉醇一线治疗ⅢB-Ⅳ期鳞状NSCLC的Ⅲ期临床研究(CameL-sq)的2年OS率(53.4% vs 35.0%)和3年OS率(42.8% vs 23.7%)数据在2022年欧洲肺癌大会(ELCC)由同济大学附属上海市肺科医院周彩存教授做了口头报告[9]。
适应证重叠是临床医生常面临的情况,而如何评估不同PD-1单抗治疗疗效成为抉择治疗方案的一个关键。
KEYNOTE-189和KEYNOTE-407的5年OS率对于指导当前国内晚期NSCLC治疗的临床实践有无意义?当前已广泛应用于临床实践的众多的PD-(L)1联合化疗方案是否都有必要跟随KEYNOTE-189和KEYNOTE-407,展示长期随访的OS和PFS数据以证明其能带来长期生存获益?
在KEYNOTE-189和KEYNOTE-407研究中那些经K药治疗后,在第5年时仍无疾病进展的患者是否可被视为临床治愈?
近日,本平台邀请周彩存教授对这些问题进行解答。
长期生存率是否是一个能真正体现免疫治疗疗效的评估指标?
周彩存教授: 在晚期肺癌的化疗和靶向治疗时代,我们都以OS作为一个抗肿瘤药物的主要评估指标。
在化疗时代,化疗带来的OS获益有限,中位OS延长仅两个月。之后,抗血管生成药物贝伐珠单抗联合化疗又把中位OS延长了两个月到半年。诸多靶向治疗药物相比化疗虽然延长了PFS,但是总体OS获益与化疗相差无几。
所以,在晚期肺癌的化疗和靶向治疗时代,我们能看到中位OS的变化,但很少能看到3年或5年的生存率数据。但是,免疫治疗带来的革命让我们看到了晚期肺癌患者的5年生存率。
5年生存率是临床治愈肿瘤的一个标准,5年生存率提高了,也意味着获得临床治愈的肿瘤病人增加了。因此,在免疫治疗时代,仅评估OS的改善显然是不充分的,我们更需要去评估PD-1治疗带来的3年和5年生存率。也就是说,在免疫治疗时代,一个方案是否能提升3年和5年生存率,能让多少病人获得临床治愈,这是比中位OS延长多少更重要的问题。
目前,对于免疫治疗,我们更需要长期随访来获得4年以及5年生存率数据。长期生存应该成为未来临床研究的一个非常重要的疗效考核指标。
KEYNOTE-189研究的PD-L1分层OS数据显示,PD-L1 TPS≥50%的晚期NSCLC的5年OS率为29.6%(对照组21.4%, HR = 0.68 [0.40-0.96]),高于PD-L1在PD-L1 TPS 1%-49%人群的19.9%(对照组7.7%, HR=0.65[0.46-0.90] 以及PD-L1 TPS <1%的人群的9.6%(对照组5.3%, HR=0.55[0.39-0.76])。KEYNOTE-407研究也显示5年OS率随着PD-L1表达降低而降低。如何看待这组数据的意义?
周彩存教授: KEYNOTE-024的5年OS数据结果显示, K药单药一线治疗PD-L1 TPS≥50%人群的5年OS率为31.9%,而KEYNOTE-189研究中相应人群的29.6%的5年OS率数据在数值上差不多,这告诉我们,针对这批人群,K药单药一线治疗足矣,无需增加化疗。
但是,在临床实践中,还是要根据具体情况具体分析。比如,如果患者的肿瘤负荷比较大,或者不抽烟,尽管PD-L1 TPS≥50%,我觉得选择K药联合化疗的治疗方案可能会更加安全。因为肿瘤负荷高,需要迅速缩瘤,K药联合化疗的起效会更快;而不抽烟的病人往往肿瘤突变负荷(TMB)比较低,用免疫单药治疗的效果可能较差,因此选择K药联合化疗可能比选择K药单药更能确保疗效。
另外一个对于临床实践具有重要的意义就是虽然PD-L1低表达或表达阴性的非鳞NSCLC人群的5年OS率虽然不及PD-L1高表达人群的5年OS率,但相比含铂化疗方案,也有明显的提高。 这组数据意味着,K药联合化疗方案也可为这批患者中的一部分人群带来5年生存,支持该治疗方案作为PD-L1表达阴性晚期NSCLC患者的标准一线治疗。
记者:这么多PD-1联合化疗方案, 医生应如何与患者沟通不同方案的疗效?是否需要告知长生存数据?
周彩存教授: 中国的晚期NSCLC患者是幸运的,因为有那么多可选择的免疫治疗方案。但方案多了,也会带来“幸福的烦恼”。医生应该向患者全面解释不同PD-1的短期、中期和长期疗效以及安全性。
当前已应用于临床实践的几个PD-1联合化疗方案的中位OS数据是差不多的,相比化疗方案带来的生存也延长和死亡风险的降低也差不多,但除了要充分告知患者这些数据,我们也要通俗易懂地告知患者每个PD-1是否有长生存的数据。
作为患者,延长几个月的生命是重要的,但更重要的是知道治疗方案有多大概率可以帮助实现3年、5年,甚至更长的生存。如果一个方案可以为患者带来20%的5年生存概率,那患者当然会选择这个方案。
那些在随访5年时,仍然未出现疾病进展的患者是否可被视为获得临床治愈?目前这个问题还没有答案。虽然,在临床实践中,我们发现活过3年的患者往往有更大的概率活过4年甚至5年,但回答这个问题,我们需要看更长时间的随访。
所以,我也期望未来,KEYNOTE-189和KEYNOTE-407能为我们带来7年和10年的OS率数据。这对于患者,对于医生和临床研究者都是具有重大意义的。
专家简介

周彩存 教授
职称:主任医师,教授,博士生导师,享受国务院特殊津贴;
单位:同济大学附属上海市肺科医院,同济大学医学院肿瘤研究所
CSCO学会任职:执行委员
其他学会任职:CSCO非小细胞肺癌专委会主委,中国医促会胸部肿瘤分会主委,上海市抗癌协会肺癌分子靶向和免疫治疗专委会主委,国际肺癌联盟(IASLC)教育委员会委员,国际肺癌联盟(IASLC)控烟委员会委员,中国抗癌协会肺癌专业委员会常委,中国抗癌协会肿瘤药物临床研究专业委员会副主任委员,中国医师协会肿瘤分会常委,上海市医师协会肿瘤分会副会长,上海市医学会肿瘤分会副主任委员
擅长领域/长期从事:肺癌精准治疗、肺癌免疫治疗、肺癌早期诊断、肺癌转化研究
主要成就:上海市领军人才,上海市重中之重呼吸病学重点学科负责人,获各类科研项目资助近20项,包括国家863计划,国家自然科学基金等。牵头或参与大型临床研究30余项,包括OPTIMAL,BEYOND等。
文 章:发表论著200余篇,Lancet Oncology, JCO, Annals of Oncology, JTO, IJC, Cancer等
获奖:中国抗癌协会科技奖一等奖、华夏医学科技奖一等奖、中华医学科技奖二等奖、上海市抗癌科技奖二等奖、上海市医学科技奖一等奖、重庆市科技进步二等奖
参考资料:
[1].M.C. Garassino et al., KEYNOTE-189 5-year update: First-line pembrolizumab (pembro) + pemetrexed (pem) and platinum vs placebo (pbo) + pem and platinum for metastatic nonsquamous NSCLC, 2022 ESMO, Abs #973MO
[2].S. Novello et al., 5-year update from KEYNOTE-407: Pembrolizumab plus chemotherapy in squamous non-small cell lung cancer (NSCLC), 2022 ESMO,Abs # 974MO
[3].Caicun Zhou et al., Camrelizumab plus carboplatin and pemetrexed versus chemotherapy alone in chemotherapy-naive patients with advanced non-squamous non-small-cell lung cancer (CameL): a randomised, open-label, multicentre, phase 3 trial, Published Online December 18, 2020 https://doi.org/10.1016/ S2213-2600(20)30365-9
[4].Zhou CC, Ren SX, Chen JH, et al. Camrelizumab or placebo plus carboplatin and paclitaxel as first-line treatment for advanced squamous NSCLC (CameL-sq): A randomized, double-blind, multicenter, phase Ⅲ trial[EB/OL]. ELCC 2021, abstract 96O.
[5].Yang YP et al., Efficacy and Safety of Sintilimab Plus Pemetrexed and Platinum as First-Line Treatment for Locally Advanced or Metastatic Non-squamous NSCLC: a Randomized, Double-Blind, Phase 3 Study (Oncology pRogram by InnovENT anti-PD-1-11), J Thorac Oncol. 2020 Oct;15(10):1636-1646. doi: 10.1016/j.jtho.2020.07.014. Epub 2020 Aug 8.
[6].Zhou C et al., Sintilimab Plus Platinum and Gemcitabine as First-Line Treatment for Advanced or Metastatic Squamous NSCLC: Results From a Randomized, Double-Blind, Phase 3 Trial (ORIENT-12). J Thorac Oncol. 2021 Sep;16(9):1501-1511. doi: 10.1016/j.jtho.2021.04.011. Epub 2021 May 25.
[7].Lu S, Yu Y, Yu X, et al. Tislelizumab+ chemotherapy vs chemotherapy alone as first-line treatment for locally advanced/metastatic non-squamous NSCLC (nsqNSCLC)[C]//ESMO Annual Meeting. 2020
[8].Wang J., Tislelizumab Plus Chemotherapy vs Chemotherapy Alone as First-line Treatment for Advanced Squamous Non-Small-Cell Lung Cancer: A Phase 3 Randomized Clinical Trial. JAMA Oncol. 2021 May 1;7(5):709-717. doi: 10.1001/jamaoncol.2021.0366.
[9].Zhou CC, First-line camrelizumab plus carboplatin and paclitaxel for advanced squamous non-small cell lung cancer: Updated overall survival results from the phase III CameL-sq trial. 3MO. 2022 ELCC.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |