*仅供医学专业人士阅读参考
大咖解读SERENA-2研究最新进展
2022年圣安东尼奥乳腺癌研讨会(SABCS)于当地时间12月6日至10日在美国圣安东尼奥盛大召开。乳腺肿瘤领域的研究进展精彩纷呈,其中,在绝经后ER+/HER2-晚期乳腺癌女性患者中比较Camizestrant与氟维司群的SERENA-2研究荣登SABCS“口头报告”专场[1],首次公布其疗效和安全性数据。医学界肿瘤频道特别邀请到SERENA-4研究中国区Leading PI、CSCO副理事长兼秘书长、解放军总医院肿瘤医学部的江泽飞教授解读SERENA-2最新研究数据,共话乳腺癌领域热点,展望未来发展。应运而生,口服SERD或可解决HR+/HER2-乳腺癌内分泌治疗的未满足之需
乳腺癌是最常见的女性恶性肿瘤,占女性新发病例的24.5%,也是全球女性癌症死亡的主要原因,占全球女性癌症死亡人数的15.5%[2]。激素受体(HR)阳性/人表皮生长因子受体2(HER2)阴性乳腺癌是最常见的乳腺癌亚型,以雌激素受体(ER)和/或孕激素受体(PR)阳性表达、HER2阴性表达为特征。其治疗长期依赖于选择性雌激素受体调节剂(SERMs,如他莫昔芬)、芳香化酶抑制剂(AIs)和选择性雌激素受体下调剂(SERD,如氟维司群)。从作用机制上看,AI通过抑制雌激素生成发挥抗肿瘤效应,他莫昔芬和氟维司群均能阻断ER。但是氟维司群具备抑制和灭活受体的双重作用,既能结合、阻断又能降解ER,机制上更优于SERM,是乳腺癌内分泌治疗的重要选择[3]。然而,注射剂型限制了氟维司群的的使用范围,促使行业开始寻找一种更加便捷、抗肿瘤疗效更强的新药物剂型,口服SERD应运而生。
Camizestrant作为新一代口服SERD,既能抑制ERα驱动的肿瘤细胞生长,又能导致ERα受体的降解,活性与氟维司群相当,对亲脂性的严格控制确保了其在口服给药时具有良好的理化性质和药代动力学特性[4],既往研究已经显示了Camizestrant单药或联合治疗在HR+/HER2-乳腺癌的有效性和安全性。本次大会首次公布Camizestrant在ER+/HER2-晚期乳腺癌中的II期研究SERENA-2的无进展生存期(PFS)、客观缓解率(ORR)及安全性数据[1]。
展现佳绩,口服SERD Camizestrant的II期研究SERENA-2达主要终点
研究方法
SERENA-2研究(NCT04214288)是一项多中心、随机、开放标签的Ⅱ期临床试验,在晚期ER+/HER2-乳腺癌患者中评估不同剂量水平Camizestrant(75mg、150mg、300mg)相比氟维司群的疗效和安全性。该研究纳入既往在晚期阶段接受过≤1线内分泌治疗和≤1线化疗的ER+/HER2-绝经后晚期乳腺癌女性患者。根据既往是否接受过CDK4/6抑制剂治疗以及是否伴有肺/肝转移进行分层,进一步探索Camizestrant的优效人群。主要终点是研究者评估的PFS。次要终点包括:ORR、OS、CBR24和安全性。
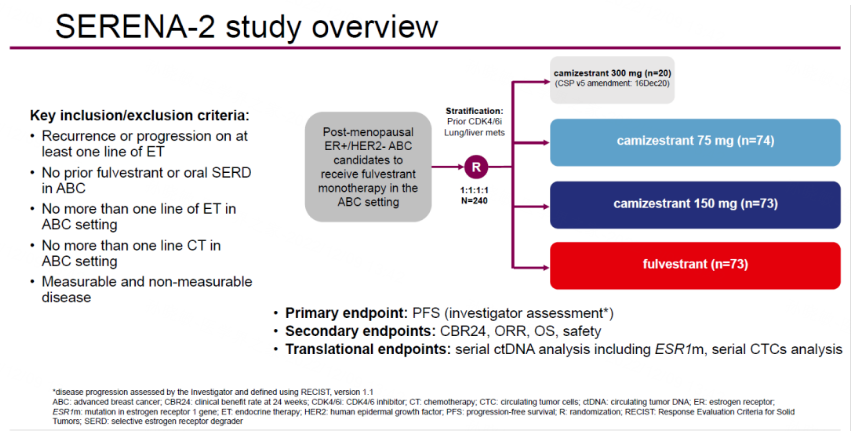
图1 研究设计
研究结果
截至2022年8月,SERENA-2研究共纳入240例患者,按照1:1:1随机分配至Camizestrant 75mg组(n=74)、Camizestrant 150mg组(n=73)和氟维司群组(n=73),由于300mg剂量组提前停止入组(n=20),因此未对Camizestrant 300mg与氟维司群进行疗效分析。三组患者人口统计学及临床特征基本相似,在总人群中,58.3%的患者伴有肺/肝转移,36.7%的患者基线存在ESR1突变。患者既往治疗的情况如下:19.2%的患者在晚期阶段接受过化疗;66.7%的患者接受过辅助内分泌治疗;68.8%的患者接受过晚期内分泌治疗,63.3%的患者使用AI。49.6%的患者接受过CDK4/6抑制剂治疗。
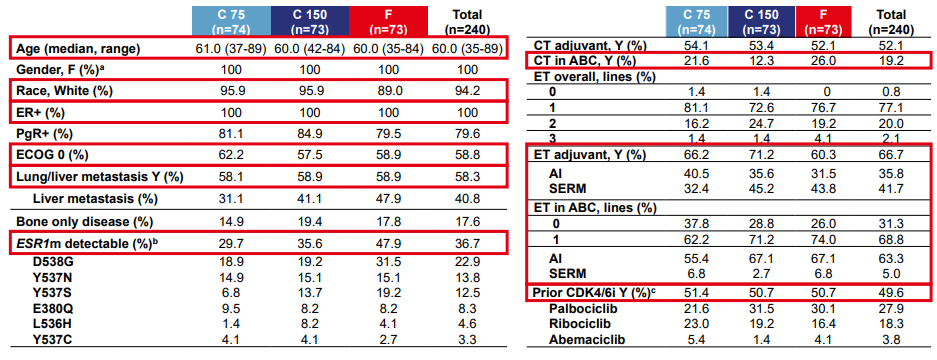
图2. 基线特征
SERENA-2研究达到主要终点。在总人群中,与氟维司群相比,两种剂量Camizestrant均可使PFS产生具有统计学意义和临床意义的改善,75mg组、150mg组和氟维司群组的中位PFS分别为7.2个月(HR=0.58,95% CI:0.41-0.81)、7.7个月(HR=0.67,95% CI:0.48-0.92)和3.7个月。
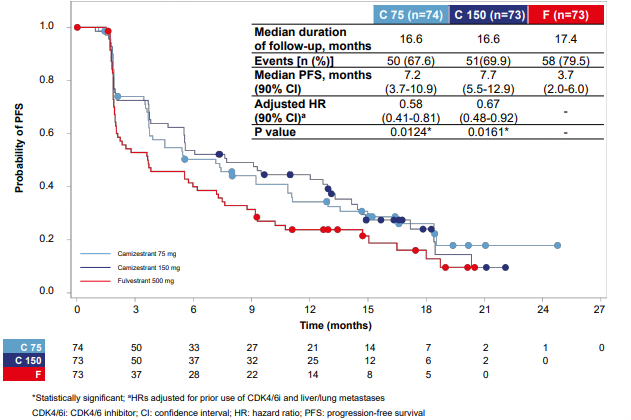
图3. 研究者评估的PFS
亚组分析显示,在既往接受CDK4/6抑制剂治疗、伴肺/肝转移、ESR1突变以及有ER驱动疾病的亚组中,PFS获益趋势与总人群一致。
与氟维司群相比,两种剂量Camizestrant均可增加ORR和CBR24,75mg组、150mg组和氟维司群组的ORR分别为15.7%、20.0%和11.8%,CBR24分别为47.3%、49.3%和38.4%。

图4. ORR及CBR24
值得一提的是,两种剂量Camizestrant均显著降低ESR1突变水平,治疗的第二周期第1天检测不到ESR1突变或接近检测不到,并维持至第7周期。氟维司群也可降低ESR1突变水平,但与Camizestrant的降低程度有显著差异。
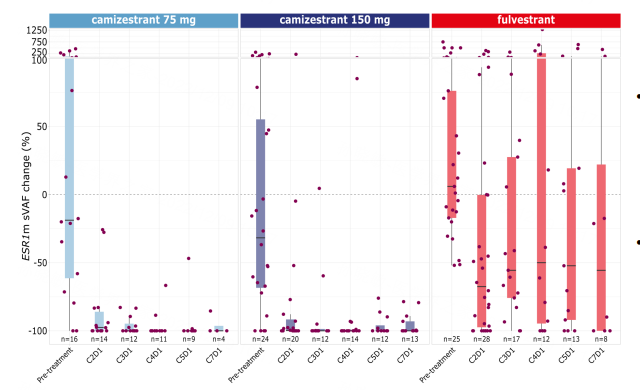
图5. ESR1突变水平变化
在安全性方面,三种剂量的Camizestrant均耐受良好。所有治疗组中≥3级治疗相关不良反应事件(TRAE)和导致停药的TRAE均较低。75mg与150mg组中,导致给药中断的TRAE发生率相似,且持续时间较短(7天和7.5天)。Camizestrant组发生率≥10%不良反应包括视觉障碍、心动过缓或窦性心动过缓、疲劳、贫血、衰弱、关节痛。
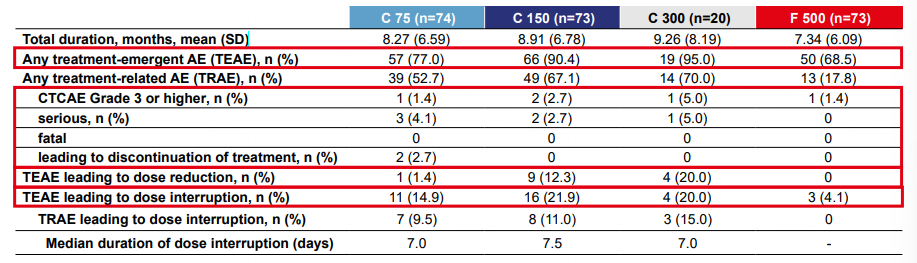
图6. 安全性总结
总体而言,SERENA-2研究证实,晚期疾病时接受过内分泌治疗或化疗的ER+/HER2-晚期绝经后乳腺癌女性患者接受Camizestrant(75mg,150mg)治疗,相较于氟维司群(500mg)取得具有统计学差异和临床意义的PFS获益。并且,Camizestrant耐受性良好,其安全性与先前试验中观察到的一致。
告往知来,Camizestrant的Ⅰ期研究数据及III期研究布局介绍
此前,Ⅰ期SERENA-1研究纳入既往接受过≥1线内分泌治疗和≤2线化疗的绝经前/后ER+/HER2-晚期乳腺癌患者,探索Camizestrant单药治疗以及与哌柏西利、阿贝西利、依维莫司或Capivasertib联合治疗的效果。结果显示,Camizestrant表现出良好的耐受性,并且单独给药或与CDK4/6抑制剂联合给药时均展现出具有前景的抗肿瘤活性。
本次SABCS大会更新了SERENA-1研究中Camizestrant联合阿贝西利组的安全性和疗效数据,入组的患者中54%接受过氟维司群治疗,75%接受过CDK4/6抑制剂,晚期阶段中位既往治疗线数为3线。截至2022年8月16日,24例患者接受Camizestrant联合阿贝西利治疗,研究结果显示,患者接受Camizestrant联合阿贝西利治疗耐受性良好,治疗期间Camizestrant无需降低剂量。联合组的PK特征与Camizestrant单药和既往阿贝西利相关研究中报道的一致,表明未发生药物相互作用(DDI)。在疗效方面,Camizestrant联合阿贝西利的ORR和CBR24分别为26.3%和66.7%[5]。总体而言,Camizestrant联合CDK4/6抑制剂具有协同增效作用,并且耐受性良好,支持此联合方案在Ⅲ期研究中的应用。

图7. PK特征
正在进行的Ⅲ期SERENA-4研究(NCT04711252)将进一步阐明Camizestrant联合哌柏西利在治疗ER+/HER2- ABC一线患者的作用。该研究是一项随机、多中心、双盲、Ⅲ期临床试验,将纳入1342例初诊或复发的ER+/HER2-晚期乳腺癌患者,既往未接受过针对局部区域复发或转移疾病的全身治疗,复发性患者必须接受AI辅助治疗或他莫昔芬治疗至少24个月且无复发。1:1随机分配至Camizestrant组(Camizestrant 75mg OD+哌柏西利125mg OD)或阿那曲唑组(阿那曲唑1mg OD+哌柏西利125mg OD)。主要终点是PFS;关键次要终点包括OS、PFS2、ORR、DoR、CBR24、至化疗的时间以及HRQoL等[6]。期待更多研究数据的公布推动Camizestrant的前线使用及获批上市,惠及更多ER+/HER2-乳腺癌患者。
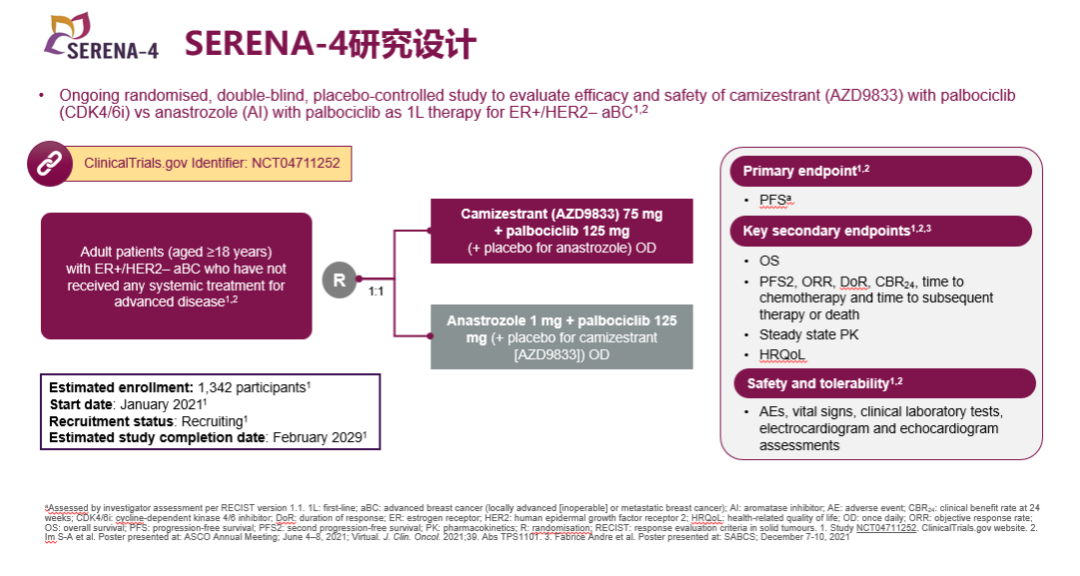
图8. SERENA-4研究设计
脱颖而出,Camizestrant成为口服SERD赛道新秀
本次更新的SERENA-2研究首次将Camizestrant与氟维司群进行头对头比较,并且在绝经后ER+/HER2-晚期乳腺癌患者显示出优于氟维司群的PFS获益,进一步验证了Camizestrant单药在ER+/HER2-晚期乳腺癌治疗中的广阔前景,将为ER+/HER2-晚期乳腺癌的治疗增加一种用药便捷的优效选择。
从目前的研究进展来看,备受关注的口服SERD还包括Amcenestrant、Giredestrant和Elacestrant等。其中,Amcenestrant和Giredestrant单药用于HR+/HER2-乳腺癌患者后线治疗的Ⅱ期探索性研究以失败告终,而Elacestrant单药治疗的中位PFS绝对获益为仅0.9个月(2.8个月 vs 1.9个月)[7]。Camizestrant在SERENA-2研究中相较于氟维司群延长了PFS为3.5-4个月,有望从口服SERD赛道中脱颖而出。
自氟维司群首个适应症获批以来,近20多年中还没有新的SERD获批上市,SERENA-2研究的成功为口服SERD的研发增加信心。随着新型口服SERDs的研发迅速从临床前实验进入III期临床研究,并取得了一些令人鼓舞的I期和II期研究初步成果,这些都表明口服SERD的应用前景值得期待。希望更多研究数据早日披露,丰富HR+/HER2-乳腺癌的内分泌治疗方案,进一步改善患者的生存预后和生活质量。
专家简介

江泽飞 教授
解放军总医院肿瘤医学部副主任
北京医学会乳腺疾病分会主任委员
中国临床肿瘤学会(CSCO)副理事长兼秘书长
中国抗癌协会 (CACA) 乳腺癌专委会候任主任委员
中国临床肿瘤学会(CSCO)乳腺癌专委会前任主任委员
参考文献
[1].Oliveira M, et al Camizestrant, a next generation oral SERD vs fulvestrant in post-menopausal women with advanced ER-positive HER2-negative breast cancer: Results of the randomized, multi-dose Phase 2 SERENA-2 trial. 2022 SABCS. CT GS3-02.
[2].Sung H, Ferlay J, Siegel RL, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. Ca Cancer J Clin. 2021;71(3):209–249.
[3].Chen YC, Yu J, Metcalfe C, et al. Latest generation estrogen receptor degraders for the treatment of hormone receptor-positive breast cancer. Expert Opin Investig Drugs. 2022 Jun;31(6):515-529.
[4].Scott JS, Moss TA, Balazs A, et al. Discovery of AZD9833, a Potent and Orally Bioavailable Selective Estrogen Receptor Degrader and Antagonist. J Med Chem. 2020 Dec 10;63(23):14530-14559.
[5].Turner N, Vaklavas C, Calvo E, et al. SERENA-1: Updated analyses from a Phase 1 study of the next generation oral selective estrogen receptor degrader camizestrant (AZD9833) combined with abemaciclib, in women with ER-positive, HER2-negative advanced breast cancer. 2022 SABCS. P3-07-28.
[6].Seock-Ah Im, Hamilton EP, Cussac AL, et al. SERENA-4: A phase 3 comparison of AZD9833 (camizestrant) plus palbociclib, versus anastrozole plus palbociclib, for patients with ER-positive, HER2-negative advanced breast cancer who have not previously received systemic treatment for advanced disease. 2021 ASCO. TPS1101.
[7].Bardia A, Neven P, Montero AJ et al. Elacestrant, an oral selective estrogen receptor degrader (SERD), vs investigator’s choice of endocrine monotherapy for ER+/HER2- advanced/metastatic breast cancer (mBC) following progression on prior endocrine and CDK4/6 inhibitor therapy: Results of EMERALD phase 3 trial. Poster presented at: 39th Annual Miami Breast Cancer Conference. March 3-6, 2022; Miami Beach, FL.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |