*仅供医学专业人士阅读参考
聚焦大会前沿,看大咖解读最新研究进展。
第45届圣安东尼奥乳腺癌大会(SABCS)于当地时间2022年12月6日至10日圆满召开。在本次大会中,许多重磅研究公布了最新成果,为乳腺癌的诊疗带来诸多新进展。尤其是抗ADC明星药物T-DXd再度重磅出击,其重磅研究DESTINY-Breast02(DB02)以“口头报告”形式首次公布研究结果,主要终点无进展生存期(PFS)和关键次要终点总生存期(OS)达到双阳性结果[1]。医学界肿瘤频道特邀张莉莉教授对相关研究发表真知灼见。
Q1:基于DESTINY-Breast01(DB01)研究的显著疗效,T-DXd加速获批用于HER2阳性晚期乳腺癌的后线治疗。DB02研究是该适应症的验证性、随机对照的Ⅲ期临床试验,其研究结果在2022 SABCS大会“口头汇报”环节首次亮相,请您介绍DB02研究的最新进展。
张莉莉教授:DB01研究显示,在既往接受过中位6线治疗的患者中,T-DXd治疗的客观缓解率(ORR)达到61%,中位PFS达到19.4个月[2]。基于此惊艳疗效,FDA于2019年12月附条件加速批准T-DXd用于至少接受过两种抗HER2的不可切除或转移性HER2阳性乳腺癌患者的治疗。但美中不足的是该研究为单臂II期研究,因此继续开展了随机对照的Ⅲ期临床试验DB02以验证T-DXd的后线治疗获益。
DB02研究是一项随机、多中心、开放的Ⅲ期试验,在既往接受过T-DM1治疗的HER2阳性晚期乳腺癌患者中比较T-DXd与医生选择的治疗(TPC,曲妥珠单抗/卡培他滨或拉帕替尼/卡培他滨)的有效性和安全性。根据激素受体状态(阳性或阴性)、既往帕妥珠单抗治疗和内脏疾病史进行分层。主要终点是盲法独立中心评估(BICR)的PFS。关键次要终点是OS,其他次要终点包括ORR、缓解持续时间(DoR)、PFS和安全性,探索性终点为临床获益率(CBR)和PFS2。

图1.DB02研究的试验设计
该研究共纳入406位患者至T-DXd组,202位患者至TPC组。入组患者为既往T-DM1经治、晚期阶段已经接受过2线及以上治疗的HER2阳性晚期乳腺癌。入组患者既往中位治疗线数为二线,几乎所有患者都接受过曲妥珠单抗和T-DM1治疗,近80%的患者接受过帕妥珠单抗治疗。
本次SABCS大会公布的研究结果显示,DB02研究达到主要终点。
与TPC组相比,T-DXd组中BICR评估的中位PFS延长了10.9个月(17.8个月vs 6.9个月),降低疾病进展或死亡风险64%;
研究者评估的PFS具有相同趋势,分别为16.7个月vs 5.5个月。
在预设亚组中,无论患者的年龄、激素受体状态、既往是否接受过帕妥珠单抗治疗、是否合并内脏转移或脑转移、既往治疗线数如何,T-DXd组与TPC组相比,PFS均有显著延长。
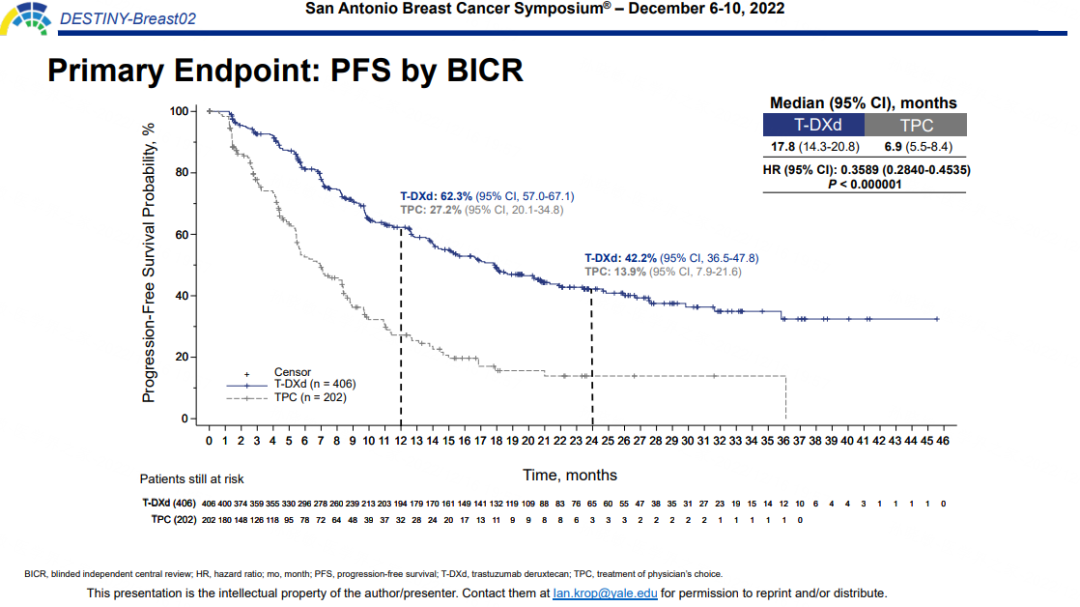
图2.DB02研究的BICR评估的PFS结果
在关键次要研究终点方面,两组中位OS分别为39.2个月和26.5个月,T-DXd组相比TPC组显著延长12.7个月,降低死亡风险达34%。尽管TPC组有25.7%的患者进展后交叉接受T-DXd治疗,T-DXd组仍取得了大幅度OS获益优势。
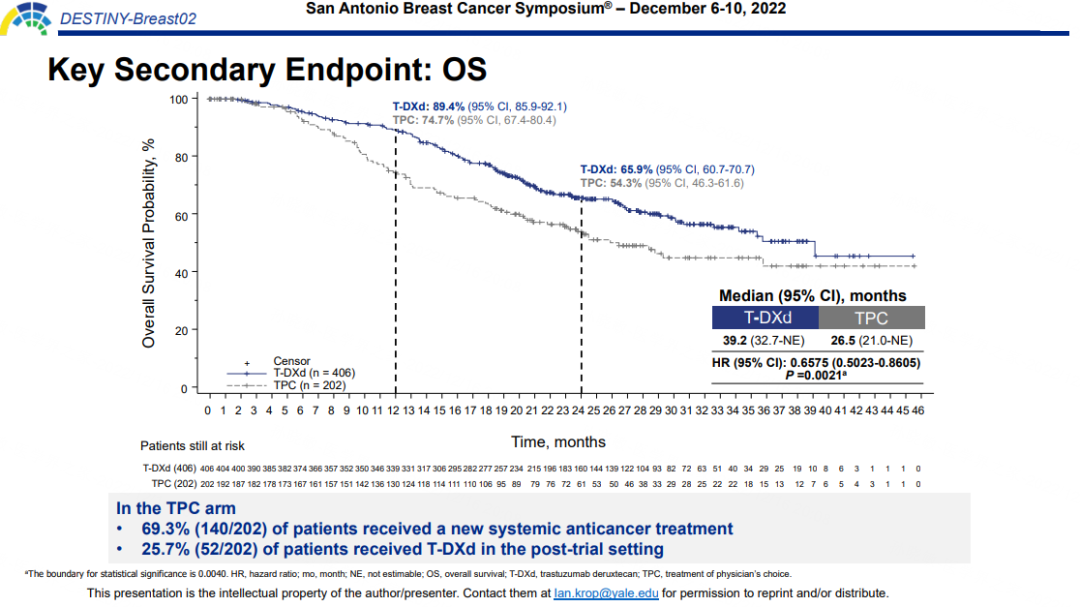
图3.DB02研究的关键次要终点OS结果
其他次要终点和探索性终点方面,T-DXd组也表现出显著性获益。两组的ORR分别为69.7%和29.2%。T-DXd组有14%的患者获得完全缓解(CR),而TPC组仅为5%。值得一提的是,T-DXd组的PFS2也显著长于TPC组(35.8个月vs 15.8个月)。
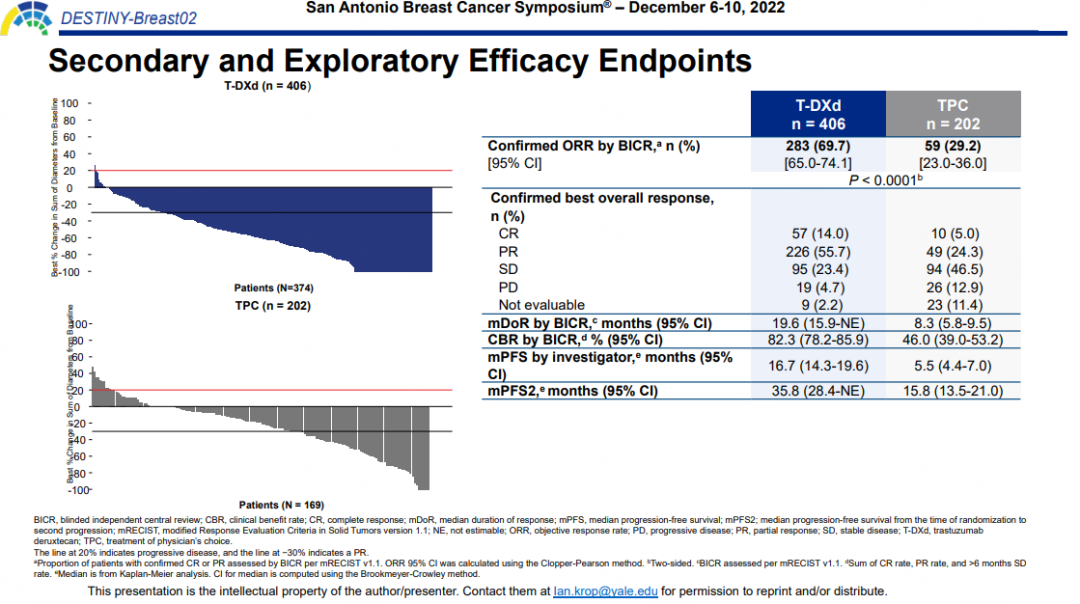
图4.DB02研究的次要终点和探索性终点结果
总体而言,作为DB01的确证性研究,DB02重现了DB01的研究成果,在Ⅲ期研究中验证了T-DXd作为HER2阳性晚期乳腺癌三线及三线以上治疗方案的有效性。
Q2:在本次SABCS大会中,DESTINY-Breast03(DB03)研究也公布了最新随访数据。基于这些研究进展,请您谈一谈如何看待T-DXd在HER2阳性晚期乳腺癌的应用价值。
张莉莉教授:DESTINY-Breast03研究是一项随机、开放、多中心III期研究,旨在头对头比较T-DXd与T-DM1在既往接受过曲妥珠单抗和紫杉类药物治疗的HER2阳性晚期二线乳腺癌患者的疗效。该研究结果于2021年ESMO大会首次报道,主要终点PFS的HR仅为0.28,显示T-DXd相比T-DM1具有显著的统计学差异和临床获益;而关键次要终点OS由于事件数较少,数据成熟度较低,两组的mOS均不可评估,HR为0.56,T-DXd有明显的获益趋势,但没有达到预先设定的统计学差异的阈值[3]。本次SABCS会议进一步更新了DB03的第二次总生存中期分析结果[4]:
T-DXd和T-DM1的中位OS均未达到(虽然仍是NR),但HR=0.64,p=0.0037,已经达到预先设计的统计学差异阈值(HR=0.652,p=0.013)。
PFS方面,T-DXd组为28.8个月,是T-DM1组的4.2倍,HR为0.33。
并且,T-DXd组的ORR高达78.5%,且1/5的患者达到CR。

图5.DB03研究中关键次要终点OS的结果
DB03研究的最新随访数据不仅显示T-DXd在二线治疗的超长PFS(28.8个月),而且OS获益与T-DM1相比也达到显著性差异,证明T-DXd的PFS获益可以转化为总生存获益,进一步夯实了T-DXd在HER2阳性晚期乳腺癌中的二线地位。
DB02研究结果显示,在T-DM1经治的HER2阳性晚期乳腺癌中,T-DXd较现有的标准治疗显著改善了PFS及OS,进一步证实了DB01研究的卓越疗效,是T-DM1经治的三线及三线以上患者的优选治疗。基于上述DB02、DB03研究成果,可以说T-DXd在HER2阳性晚期乳腺癌的治疗中占有非常重要的地位。
值得一提的是,T-DXd还布局了DESTINY-Breast09研究,评估T-DXd单药或联合帕妥珠单抗对比当前一线标准治疗方案(THP,曲帕+化疗)的有效性和安全性,是首个挑战THP一线标准治疗的Ⅲ期研究。基于T-DXd的创新结构优势以及既往DB01、DB02、DB03研究的突破性获益,我们相信T-DXd也将在HER2阳性晚期乳腺癌一线治疗中取得成功,进一步丰富一线用药选择。另外,DESTINY-Breast11(新辅助)和DESTINY-Breast05(辅助)研究旨在探索T-DXd在HER2阳性早期乳腺癌的价值,这些研究结果非常值得期待。
Q3:药物安全性是治疗需要考虑的重要因素,结合既往研究进展,请您谈一谈T-DXd的整体安全性如何。
张莉莉教授:现有的临床研究数据显示,T-DXd的常见不良反应以消化道、血液学以及乏力、脱发等一般性不良反应为主。对于临床医生而言,针对这些不良反应的准确识别和有效管理可以说已经非常熟悉,经验相当丰富。
接受T-DXd治疗时,需要特别关注的不良反应主要为间质性肺病(ILD),DB01研究中,T-DXd组有15.8%的患者发生与治疗相关的ILD,多数为1-2级,3-5级的发生率为3.3%[2]。与DB01相比,在DB02研究中观察到的ILD事件较少,整体ILD事件发生率为10.4%,多数为1-2级,3-5级的发生率为1.2%[1]。DB03研究的最新数据显示,随着随访时间延长,ILD的发生率由此前的10.5%增加至15.2%,但新增ILD事件中均为1-2级,仍然只有2位患者发生3级ILD(发生率为0.8%),没有4级或5级ILD事件发生[4]。可以看出,随着治疗线数的前移,ILD事件的发生率,尤其是3-5级发生率,呈现出降低的趋势。
总体而言,随着相关认识的提高和用药经验的积累,T-DXd的相关不良反应是可防可控的。在临床工作中,对ILD应该保持警惕,及早识别高危人群,做到早预防、早发现、早治疗,这有助于减少ILD的发生率和致死率,改善患者预后,提高其生活质量。
Q4:您怎么看待DESTINY-Breast03研究中公布的PFS2数据?以及,您如何看待不同ADC药物的排兵布阵问题?
张莉莉教授:在DB03研究中,更新的数据显示T-DXd相比T-DM1的OS延长达到显著差异,证明了其对长期生存获益。此外,T-DXd和T-DM1组的PFS2分别是40.5个月 vs 25.7个月,从这一数据可以看出,T-DXd放在前线治疗使用,并未损害后线治疗的获益。DB03研究的更新结果确证了T-DXd在二线治疗的标准地位。
此前,基于DB03研究的早期结果,T-DXd二线治疗HER2阳性晚期乳腺癌相比T-DM1大幅度提升生存获益,ESMO、ABC6、NCCN和ASCO等国际权威指南均推荐T-DXd作为HER2阳性晚期乳腺癌的二线治疗的优选方案,取代T-DM1成为全球二线治疗新的标准。而在二线应用T-DXd治疗进展后如何选择后续治疗方案,将是临床面临的一个重要问题。在DB03研究的后续治疗分析中,T-DXd组后续接受的治疗包括曲妥珠单抗、T-DM1、帕妥珠单抗、抗HER2 TKI等。其中,35.2%的患者在疾病进展后接受了T-DM1的治疗,表明T-DM1可能是T-DXd治疗进展后的可选方案之一,当然这部分亚组患者的治疗获益尚不明确,非常值得进一步研究。而对于T-DM1经治的患者,DB02研究结果显示了T-DXd的显著获益,因此,T-DXd可作为T-DM1经治患者的优选治疗。
关于ADC药物排兵布阵的问题,可以根据不同ADC药物各自的组成、作用机制、临床研究的结果、药物的可及性、安全性及耐药机制的研究等加以考量。未来会有更多的ADC药物问世,排兵布阵也不是一成不变的,需要在临床上不断探索最佳的治疗模式。
专家简介

张莉莉 教授
江苏省肿瘤医院内科 主任医师,硕士生导师,病区主任
中国抗癌协会乳腺癌专业委员会委员
中国临床肿瘤学会乳腺癌专家委员会委员
江苏省肿瘤专业质控中心乳腺癌质控专家委员会主任委员
江苏省医学会肿瘤化疗与生物治疗分会乳腺癌学组副组长
中国医师协会肿瘤医师分会乳腺癌学组委员
中国女医师协会乳腺专业委员会常委
江苏省肿瘤防治联盟乳腺癌专家委员会委员
主要从事乳腺癌的临床、科研及教学工作,擅长乳腺癌的内科诊治,主持及参与多项乳腺癌相关的科研课题
承担多项乳腺癌相关新药、新方案的国际及国内多中心临床研究
参考文献:
[1]Krop I,Yeon H.Park YH,Kim SB,et al.Trastuzumab deruxtecan vs physician’s choice in patients with HER2+unresectable and/or metastatic breast cancer previously treated with trastuzumab emtansine:primary results of the randomized,phase 3 study DESTINY-Breast02.2022 SABCS.GS2-01.
[2]Modi S,Saura C,Yamashita T,et al.Trastuzumab Deruxtecan in Previously Treated HER2-Positive Breast Cancer.N Engl J Med.2020 Feb 13;382(7):610-621.
[3]Cortés J,Kim S,Chung W,et al.Trastuzumab deruxtecan(T-DXd)vs trastuzumab emtansine(T-DM1)in patients(Pts)with HER2+metastatic breast cancer(mBC):Results of the randomized phase III DESTINY-Breast03 study.2021 ESMO.LBA1.
[4]Hurvitz SA,Chung WP,Im SA,et al.Trastuzumab deruxtecan versus trastuzumab emtansine in patients with HER2-positive metastatic breast cancer:Updated survival results of the randomized,phase 3 study DESTINY-Breast03.2022 SABCS.GS2-02
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |